题目内容
1.硬水中含有可溶性钙和镁的化合物,会给生活和生产带来许多影响.下列方法中可用于软化硬水且软化效果最好的是( )| A. | 蒸馏 | B. | 煮沸 | C. | 沉淀 | D. | 过滤 |
分析 根据已有的知识进行分析,最高程度的净水就是得到的水中不含有任何杂质.
解答 解:A、蒸馏得到的是蒸馏水,不含有任何杂质,是净水的最高程度,故A正确;
B、煮沸只能除去水中的部分杂质,不能得到纯水,故B错误;
C、沉淀只能除去水中的不溶性固体杂质,不能除去可溶性钙镁化合物,故C错误;
D、过滤能除去水中的不溶性固体小颗粒,不能除去水中的可溶性钙镁化合物,故D错误;
故选A.
点评 本题考查了净水的方法,完成此题,可以依据每种方法除去的杂质的类别进行.

练习册系列答案
相关题目
11.科学研究发现:金星大气层的成分之一是三氧化二碳(C2O3),实验证明三氧化二碳的化学性质与一氧化碳相似.下列关于三氧化二碳的说法中,不正确的是( )
| A. | C2O3能使澄清石灰水变浑浊 | B. | C2O3的密度比空气的密度大 | ||
| C. | C2O3在一定条件下能还原氧化铁 | D. | C2O3在O2中充分燃烧的产物为CO2 |
12.日常生活中的下列变化,一定发生化学变化的是( )
| A. | 水蒸发 | B. | 用活性炭除去冰箱中的异味 | ||
| C. | 节日燃放烟花 | D. | 自行车胎充气过多爆炸 |
9.欲将下列物质中所含杂质除去,所选试剂正确的是( )
| 序号 | 物质 | 所含杂质 | 除杂试剂 |
| A | HCl | CO2 | 适量NaOH溶液 |
| B | CaCO3 | CaCl2 | 适量稀盐酸 |
| C | 盐酸 | 稀硫酸 | 适量AgNO3溶液 |
| D | ZnSO4溶液 | CuSO4溶液 | 适量锌粉 |
| A. | A | B. | B | C. | C | D. | D |
13.以下自然资源的利用过程中,发生了化学变化的是( )
| A. | 海水晒盐 | B. | 风力发电 | ||
| C. | 太阳能取暖 | D. | 煅烧石灰石制生石灰 |
2.氢氧化钠是重要的工业原料,以下是有关它的性质实验.
(1)如图1所示,反应后溶液(编号为 a)中溶质的组成情况可能有3种.
为证明溶液 a 中可能含有的溶质,进行了如下实验:
①确定溶液 a 中是否含有氢氧化钠
②确定溶液a中是否含有盐酸
i.上述方案中有一个设计不合理,指出不合理的实验方案编号及原因方案一不合理、生成的氯化钠也会与硝酸银生成白色沉淀;
ii.采取正确的实验方案,进行实验,根据现象得到的结论是溶液中含有稀盐酸,且溶质是氯化钠和氯化氢;ⅲ.欲从溶液a中得到纯净的氯化钠,可以采取的实验操作是蒸发结晶.
(2)利用如图2装置验证氢氧化钠能与二氧化碳反应.(装置气密性良好)
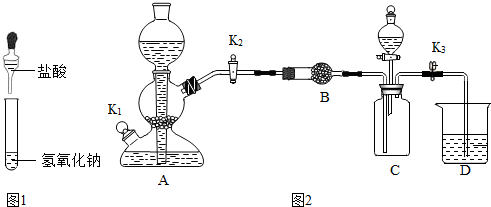
①装置A用于制取二氧化碳,打开K2、K3,当D中紫色石蕊试液变红色,可确定C中收集满二氧化碳.
②甲同学打开装置 C 中分液漏斗活塞,将 8mL 室温时氢氧化钠饱和溶液滴入 C 中,然后关闭活塞,观察到 D 中石蕊试液倒流至 C 中.甲同学得出结论,氢氧化钠能与二氧化碳反应.
③乙同学认为上述现象不足以证明氢氧化钠能与二氧化碳发生反应,还应利用上述装置补充一个对比实验.
结论:氢氧化钠能与二氧化碳反应,写出该反应的化学反应方程式2NaOH+CO2=Na2CO3+H2O.
(1)如图1所示,反应后溶液(编号为 a)中溶质的组成情况可能有3种.
为证明溶液 a 中可能含有的溶质,进行了如下实验:
①确定溶液 a 中是否含有氢氧化钠
| 步骤 | 现象 | 结论 |
| 取少量溶液a,滴加氯化铜溶液 | 溶液中无蓝色絮状沉淀 | 不含氢氧化钠 |
| 方案 | 步骤 | 现象 |
| 一 | 取少量溶液a,滴加硝酸银溶液 | 产生白色沉淀 |
| 二 | 取少量溶液a,加入镁粉 | 产生气泡 |
ii.采取正确的实验方案,进行实验,根据现象得到的结论是溶液中含有稀盐酸,且溶质是氯化钠和氯化氢;ⅲ.欲从溶液a中得到纯净的氯化钠,可以采取的实验操作是蒸发结晶.
(2)利用如图2装置验证氢氧化钠能与二氧化碳反应.(装置气密性良好)

①装置A用于制取二氧化碳,打开K2、K3,当D中紫色石蕊试液变红色,可确定C中收集满二氧化碳.
②甲同学打开装置 C 中分液漏斗活塞,将 8mL 室温时氢氧化钠饱和溶液滴入 C 中,然后关闭活塞,观察到 D 中石蕊试液倒流至 C 中.甲同学得出结论,氢氧化钠能与二氧化碳反应.
③乙同学认为上述现象不足以证明氢氧化钠能与二氧化碳发生反应,还应利用上述装置补充一个对比实验.
| 液体 | 步骤 | 现象 |
| 水 | 打开分液漏斗活塞,加入液体后关闭活塞 | D中导管先有气泡冒出,后D中石蕊试液倒流较少或D中导管倒吸一段水柱 |
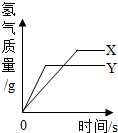 回答下列有关金属的问题:
回答下列有关金属的问题: