题目内容
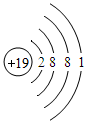
9.下面是几种粒子的结构示意图,请回答下列问题:
(1)属于同种元素的是⑤⑥(填序号);
(2)化学性质相似的是①③(填序号);
(3)上述粒子可以通过得到电子变成原子的是④(填序号);
(4)由所提供的粒子中能直接构成的化合物的化学式是MgCl2,它的构成与氯化钠相似,则它是由Mg2+、Cl-(填粒子符号)构成的.
分析 (1)根据元素的概念:具有相同核电荷数(核内质子数)的一类原子的总称,则同种元素其核内质子数相同;
(2)化学性质与原子的最外层电子数有关,最外层电子数相同,化学性质相似,且最外层电子数是8则稳定,当第一层作为最外层时,2个电子就稳定;
(3)阳离子是原子失去电子形成,则该粒子得到电子又可变为原子;
(4)根据粒子所带电荷可推测其化合价,进而书写物质的化学式,并据离子符号书写方法解答.
解答 解:(1)质子数相同即为同种元素,所以⑤⑥质子数相同,为同种元素;
(2)化学性质与粒子的最外层电子数有关,①的原子只有1个电子层,最外层电子数是2,达稳定结构,③的原子最外层电子数是8,也达到稳定结构,二者的化学性质相似;
(3)④表示的粒子得到2个电子又能变成原子;
(4)④的粒子带2个单位正电荷,其化合价是+2价,该元素是12号元素,是镁元素,⑥的粒子带1个单位负电荷,其化合价是-1价,该元素是17号元素,氯元素,二者形成化合物的化学式是MgCl2,镁离子带2个单位正电荷,离子符号是Mg2+,氯离子带一个单位的负电荷,离子符号是Cl-;
故答案为:
(1)⑤⑥;
(2)①③;
(3)④;
(4)MgCl2;Mg2+、Cl-.
点评 了解核外电子在化学反应中的作用;了解原子结构示意图与离子结构示意图的特点,化学式的书写方法、离子的书写方法等知识,才能结合题意正确解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列化学变化中吸收热量的是( )
| A. | 高温煅烧石灰石 | B. | 红磷在氧气中的燃烧 | ||
| C. | 镁和稀盐酸的反应 | D. | 生石灰与水反应 |
20.室内的电线或家用电器因使用不慎而起火时,最好的灭火方法是( )
| A. | 迅速用水泼灭 | B. | 迅速用湿棉被捂住 | ||
| C. | 迅速拉断电线再泼水 | D. | 迅速切断电源然后灭火 |
18.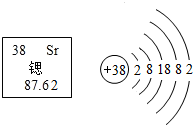 据媒体报道,锶晶体格钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒.如图为锶元素的相关信息,下列说法正确的是( )
据媒体报道,锶晶体格钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒.如图为锶元素的相关信息,下列说法正确的是( )
 据媒体报道,锶晶体格钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒.如图为锶元素的相关信息,下列说法正确的是( )
据媒体报道,锶晶体格钟是一种新型原子钟,其准确度高得惊人,它能在50亿年间不慢一秒也不快一秒.如图为锶元素的相关信息,下列说法正确的是( )| A. | 锶的相对原子质量为87.62g | |
| B. | 该元素的核电荷数为38 | |
| C. | 锶原子易得到两个电子形成离子Sr2+ | |
| D. | 锶属于非金属元素,位于第五周期 |
19.“远离毒品,珍爱生命”,每年的6月26日是国际禁毒日,一种新型毒品K粉的主要成分是盐酸氯胺酮(化学式为C13H16ONCl),它会对大脑造成永久损害.下列叙述中错误的是( )
| A. | K粉中含有盐酸 | |
| B. | 盐酸氯胺酮由五种元素组成 | |
| C. | 盐酸氯胺酮分子中,C、H、O、N、Cl 的原子个数比为13:16:1:1:1 | |
| D. | 盐酸氯胺酮中氢元素与氧元素的质量分数相同 |
 如图所示,打开分液漏斗,使其中的无色液体与试管中的固体接触反应,可观察到气球胀大现象,请分别写出一个符合图中现象和下列要求的化学方程式:
如图所示,打开分液漏斗,使其中的无色液体与试管中的固体接触反应,可观察到气球胀大现象,请分别写出一个符合图中现象和下列要求的化学方程式: 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法正确的是B
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法正确的是B 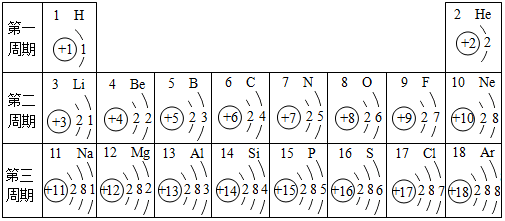
 .
.
