题目内容
在实验室用KClO3和MnO2制取氧气.为了分离出二氧化锰设计了下列程序:(提示:KCl溶于水,MnO2难溶于水)
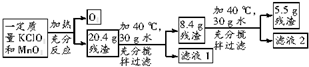
根据图示回答下列问题:
(1)写出用KClO3和MnO2制取氧气的化学反应方程式为 ;
(2)判断5.5g残渣的成分是 ;
(3)制取氧气的总质量是 ;
(4)用氧气质量求氯酸钾质量(x)的比例式为 .

根据图示回答下列问题:
(1)写出用KClO3和MnO2制取氧气的化学反应方程式为
(2)判断5.5g残渣的成分是
(3)制取氧气的总质量是
(4)用氧气质量求氯酸钾质量(x)的比例式为
考点:混合物的分离方法,实验室制取氧气的反应原理,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:物质的分离和提纯
分析:根据实验室制用KCl03和Mn02制取氧气的化学方程式和溶质的质量分数进行分析解答本题.
解答:解:(1)实验室制用KCl03和Mn02制取氧气的化学方程式:2KClO3
2KCl+3O2↑.
故填:2KClO3
2KCl+3O2↑.
(2)根据实验室制用KCl03和Mn02制取氧气的化学方程式:2KClO3
2KCl+3O2↑可知氯酸钾反应后生成物是可溶于水的氯化钾和氧气,与二氧化锰的混合物,第一次加30g水溶解的氯化钾的质量为12g,说明第二次加的10g水最多溶解4g,而实际第二次加10g水只溶解了3g,说明氯化钾全部溶解,因此剩余的物质为二氧化锰,
故填:MnO2;
(3)根据生成物氯化钾的质量:(20.4g-8.4g)+(8.4g-5.5g)=14.9g
设制取氧气的总质量为 y,氯酸钾质量为 x
2KClO3
2KCl+3O2↑
245 149 96
x 14.9g y
=
,则y=9.6g
故填:9.6 g;
(4)根据氧气质量求氯酸钾质量(x)的.比例式为
=
,
故填:
=
.
| ||
| △ |
故填:2KClO3
| ||
| △ |
(2)根据实验室制用KCl03和Mn02制取氧气的化学方程式:2KClO3
| ||
| △ |
故填:MnO2;
(3)根据生成物氯化钾的质量:(20.4g-8.4g)+(8.4g-5.5g)=14.9g
设制取氧气的总质量为 y,氯酸钾质量为 x
2KClO3
| ||
| △ |
245 149 96
x 14.9g y
| 149 |
| 14.9g |
| 96 |
| y |
故填:9.6 g;
(4)根据氧气质量求氯酸钾质量(x)的.比例式为
| 245 |
| 96 |
| x |
| 9.6g |
故填:
| 245 |
| 96 |
| x |
| 9.6g |
点评:本题考查根据实验室制用KClO3和MnO2制取氧气的化学方程式和溶质的质量分数进行解题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质属于纯净物的是( )
| A、空气 | B、液氧 |
| C、石灰石 | D、冰红茶 |
 小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强通过计算氮的质量分数发现该广告是虚假广告.
小强同学在公共场所围墙上看到一则化肥广告(如图).回校后,小强通过计算氮的质量分数发现该广告是虚假广告.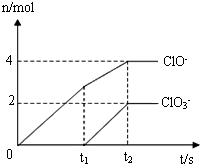 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生反应的反应均为放热反应).生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示.已知,生成ClO3-离子的反应为:6Ca(OH)2+6Cl2=5CaCl2+Ca(ClO3)2+6H2O.
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生反应的反应均为放热反应).生成物中有三种含氯元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示.已知,生成ClO3-离子的反应为:6Ca(OH)2+6Cl2=5CaCl2+Ca(ClO3)2+6H2O.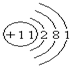 根据钠原子结构示意图;回答下列问题:
根据钠原子结构示意图;回答下列问题: