题目内容
1.水与人类的生活和生产密切相关.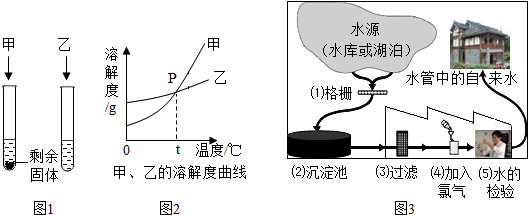
(1)水是很好的溶剂.常温下,将1克下列物质分别加入100g水中,充分搅拌(或振荡),能配制成溶液的是B.
A.汽油 B.蔗糖 C.氢氧化镁 D.氧化铁
(2)图2为甲、乙两种固体物质在水中的溶解度曲线.
①曲线上P点的含义是t℃时,甲和乙的溶解度相等.
②某温度下,向分别盛有等质量甲、乙两种固体物质的试管中,加入10g水,使其充分溶解,观察到如右图1所示的现象.则该实验的温度<(填“>”、“<”或“=”)t°c.要使甲继续溶解,又不改变溶液中溶质的质量分数,可采取的方法是升高温度.
(3)图3表示某市饮用水的净化过程,请回答下列问题:
①天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是蒸馏.
②硬水给生活和生产带来很多麻烦,生活中常用加热煮沸的方法来降低水的硬度.
③饮用水消毒剂除了目前采用的液氯以外,补充了氯胺(NH2Cl)、臭氧(O3)等.O3中氧元素的化合价是0.NH2Cl中氯元素与氢元素的质量比是71:4.
分析 (1)不能溶于水的物质不能和水形成溶液;
(2)根据溶解度曲线可以判断相关方面的问题;
(3)蒸馏可以得到蒸馏水;
加热煮沸可以降低水的硬度;
单质中,元素的化合价规定为零;
根据物质的化学式可以计算组成元素质量比.
解答 解:(1)因为汽油、氢氧化镁和氧化铁都是不溶于水的物质,因此不能和水形成溶液,蔗糖易溶于水,能和水形成溶液.
故选:B.
(2)①曲线上P点的含义是t℃时,甲和乙的溶解度相等.
故填:t℃时,甲和乙的溶解度相等.
②某温度下,向分别盛有等质量甲、乙两种固体物质的试管中,加入10g水,使其充分溶解,观察到如右图1所示的现象,说明该温度下,甲的溶解度小于乙的溶解度,对比溶解度曲线可知,该实验的温度小于t℃;
甲的溶解度随着温度升高而增大,要使甲继续溶解,又不改变溶液中溶质的质量分数,可采取的方法是升高温度.
故填:<;升高温度.
(3)①天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是蒸馏,因为蒸馏几乎可以得到纯净水.
故填:蒸馏.
②加热煮沸时,水中的钙离子、镁离子能够以碳酸钙沉淀、氢氧化镁沉淀的形式从水中析出,从而降低水的硬度.
故填:加热煮沸.
③臭氧属于单质,O3中氧元素的化合价是0;
NH2Cl中氯元素与氢元素的质量比是:35.5:(1×2)=71:4.
故填:0;71:4.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

某实验小组同学欲通过实验探究金属的性质。
【实验目的】证明金属活动性强弱:Al > Cu
【设计并实施实验】小组内的3位同学分别做了下述实验:
实验 | 现象 | |
甲 | 将铝片直接放入到稀CuCl2溶液中 | 一段时间后才出现了预期的实验现象 |
乙 | 将用砂纸打磨过的铝片放入稀CuCl2溶液(与甲实验浓度相同)中 | 十几秒内即观察到明显现象。 |
丙 | 将用砂纸打磨过的铝片放入稀CuSO4溶液中 | 在与乙相同的时间内没有观察到明显现象 |
(1)实验中,预期的实验现象是________。
(2)对比甲、乙两位同学的实验,推测甲同学开始时没有观察到明显实验现象的原因是________。
该小组同学进一步对实验进行探究。
【提出问题】为什么打磨过的铝片放入到CuCl2溶液和CuSO4溶液中观察到的现象不同呢?
【微观探析】查阅资料可知两个反应的微观示意图如下。
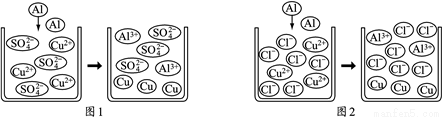
(3)图1反应的化学方程式为________;Al和CuCl2溶液、CuSO4溶液反应的微观本质是Al和Cu2+反应生成 Al3+和______ 。
【提出猜想】根据上述图示,小组同学提出了如下猜想。
猜想1:产生现象不同的原因是CuCl2溶液比CuSO4溶液中含有的Cu2+浓度大。
猜想2:溶液中Cl-对Al和Cu2+反应有促进作用。
猜想3:溶液中SO42-对Al和Cu2+反应有阻碍作用。
【设计并实施实验】
序号 | 实验方案及操作 | 现象 | 结论 |
1 | 乙、丙两位同学取Cu2+浓度相同的CuCl2溶液和CuSO4溶液重复实验。 | 与上述乙、丙同学实验现象相同 | 猜想1______(填“成立”或“不成立”) |
2 |
| 在同一时间内,③最快产生现象,②次之,①无明显现象 | 猜想2成立 |
(5)甲同学认为通过实验2得到的结论证据不充足,其理由是溶液中的__________ 对实验可能有干扰。
(6)丙同学通过查阅资料排除了上述干扰,并模仿实验2又设计了一组3支试管的实验,证明了猜想3也成立。请在下列方框中画出实验设计图示。__________

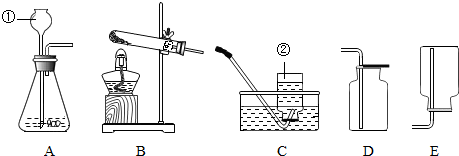
九年级(三)班化学兴趣小组为测定大理石中碳酸钙的含量,如下图所示:
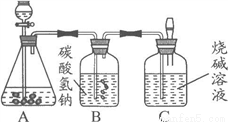
将过量的稀盐酸加入到20 g大理石中(其他成分不与盐酸反应),把产生的CO2气体用足量的烧碱溶液吸收,同时测量C瓶烧碱溶液增加的质量,结果如下表所示:
时间 / 分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
C增加质量/C | 0 | 3.0 | 5.0 | 6.0 | 6.6 | x | 6.6 |
(1)上表中,第10分钟时,x= 。
(2)计算大理石样品中碳酸钙的质量分数。
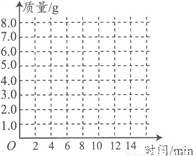
(3)请在下图的坐标纸上,以时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线;
(4)B中所装药品为碳酸氢钠溶液,作用是吸收可能挥发的HCl气体,你认为对测量结果有没有影响? (填“有”或“没有”)
| A. | 均一的、稳定的液体一定是溶液 | |
| B. | 汽油洗涤衣服上的油污,是因为汽油的乳化作用 | |
| C. | 硫酸铜溶液中的溶质是铜 | |
| D. | 乙醇和水可以以任意比互溶 |

 多角度认识物质,能帮助我们更全面了解物质世界.
多角度认识物质,能帮助我们更全面了解物质世界.