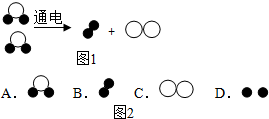
题目内容
18.已知某无色溶液里含有盐酸,则该溶液中还可能有的物质是CaCl2(填化学式).A.氯化钙 B.硝酸银 C.碳酸钠 D.氢氧化铜
上述物质不能存在于该无色溶液中的原因是(写出化学方程式)
(1)AgNO3+HCl=AgCl↓+HNO3;
(2)Na2CO3+2HCl=2NaCl+H2O+CO2↑ (写出两个就可).
分析 A、碳酸根离子会与酸反应生成二氧化碳和水,
B、氢氧根离子会和氢离子发生中和反应生成水,
C、氯化锌是盐,和盐酸不会反应,
D、铜离子显蓝色.
根据质量守恒定律正确书写化学方程式.
解答 解:A、氯化钙和盐酸不会反应,因为它们之间的反应不满足复分解反应的条件,故A正确,
B、硝酸银中含有银离子,会与氯离子发生反应生成氯化银沉淀,所以不能存在于盐酸中,故B错误,
C、纯碱中含有碳酸根离子,会与氢离子反应生成二氧化碳和水,所以不能存在于盐酸中,故C不正确,
D、氢氧化铜中的铜离子显蓝色,溶液是无色的,氢氧根离子能与氢离子结合生成水,故D错误,
故选:CaCl2.
反应的方程式:(1)AgNO3+HCl=AgCl↓+HNO3;
(2)Na2CO3+2HCl=2NaCl+H2O+CO2↑.
点评 本题主要考查了离子之间的共存问题,以及初中阶段的带色离子,要加强记忆.

练习册系列答案
相关题目
9.联合国决议将每年的4月22日定为“世界地球日”.活动旨在唤起人类爱护地球、保护家园的意识,以促进资源开发与环境保护的协调发展,进而改善地球的整体环境,下列不符合主旨的做法是( )
| A. | 垃圾分类回收处理,保护自然生态环境 | |
| B. | 禁止使用化石燃料,以减少雾霾的形成 | |
| C. | 合理开采和利用稀土资源,保障科学发展 | |
| D. | 促进生态文明,共建美丽中国 |
6. 为测定锌铜合金中锌的含量,取该合金放入盛有稀硫酸的锥形瓶中(如图),发生反应.多次实验后,取平均值所得数据如下表:
为测定锌铜合金中锌的含量,取该合金放入盛有稀硫酸的锥形瓶中(如图),发生反应.多次实验后,取平均值所得数据如下表:
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)生成氢气的质量为0.4g.
(2)该合金中锌的质量分数.
 为测定锌铜合金中锌的含量,取该合金放入盛有稀硫酸的锥形瓶中(如图),发生反应.多次实验后,取平均值所得数据如下表:
为测定锌铜合金中锌的含量,取该合金放入盛有稀硫酸的锥形瓶中(如图),发生反应.多次实验后,取平均值所得数据如下表:| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌铜合金质量 | |
| 342.10g | 16.00g | 357.70g |
(1)生成氢气的质量为0.4g.
(2)该合金中锌的质量分数.
10.如图是某物质的分子结构示意图,关于该物质的说法正确的是( )
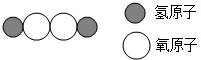

| A. | 它是由氢气和氧气组成的 | B. | 它是由氢分子和氧分子构成的 | ||
| C. | 它是由氢元素和氧元素组成 | D. | 它是由2个氢原子和2个氧原子构成 |