��Ŀ����
10���û�ѧ֪ʶ�ش��������⣮��1������������FeSO4��������ɫ��б�ᾧ�����������ζ�������������ȱ����ƶѪ֢���dz��õIJ�������������������Ԫ�صĻ��ϼ�Ϊ+2��
��2�����������г����綯���Ľ�������϶���һ��Ư���IJ�ɫ���ᣬ���������⣬�������Ҫ��Ŀ���Ƿ�ֹ��������ʴ��
��3����ϴ�Ӽ�ȥ����������Ϊϴ�Ӽ������黯���ܣ�
��4��С���Ҳ˵�����߲�Ҷ�ӷ����ˣ��������ȥ��̼���ⰷ��NH4HCO3����ʩ�ã������������̵�ʱ��̼����笠պ�ȱ�����ϰ彨���������أ�ѡ����ء����Ȼ��ء�����Ҳ������̼�������ͬ�����ã�
��5�����Ρ���ɫ��Ⱦ���Ĵ�ʩ��ʹ�ÿɽ�������ϣ�����дһ�㼴�ɣ�
���� ��1�����ݻ������������Ļ��ϼ۵Ĵ�����Ϊ����н��
��2�����ݷ�ֹ������ķ������н��
��3������ϴ�Ӽ������黯���ý��н��
��4�������߲�Ҷ�ӷ��ƣ�Ӧ��ʩ�ӵ��ʽ��н��
��5�����ݷ��Ρ���ɫ��Ⱦ���Ĵ�ʩ���н��
��� �⣺��1�������ڻ������������Ļ��ϼ۵Ĵ�����Ϊ�㣬��FeSO4���������-2�ۣ����ԣ���Ԫ�صĻ��ϼ�Ϊ+2�ۣ����+2��
��2�����������г����綯���Ľ�������϶���һ��Ư���IJ�ɫ���ᣬ���������⣬�������Ҫ��Ŀ���Ƿ�ֹ��������ʴ�������ֹ��������ʴ��
��3����ϴ�Ӽ�ȥ����������Ϊϴ�Ӽ������黯���ܣ�����黯��
��4���߲�Ҷ�ӷ��ƣ�Ӧ��ʩ�ӵ��ʣ��������ڵ��ʣ����Կ��������ش���̼����泥�������أ�
��5�����Ρ���ɫ��Ⱦ���Ĵ�ʩ��ʹ�ÿɽ�������ϣ����ʹ�ÿɽ�������ϣ�
���� ������Ҫ�������������йصĻ�ѧ֪ʶ���ѶȲ�����Ҫ��ǿʶ�Dz�����ȷ���

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
1���ӱ�ˮ����2016��1��6��¶�����š��������ȡ�֮�Ƶĺӱ��ȷ��н�������Эͬ��չս�ԵĻ��������оvɫ��չ�����벢�٣����о���֮��ˮ��̬���������ƣ�ˮ�����DZ������Դ�����������У����ϱ���ˮ��Դ���������ǣ�������
| A�� | ˮ��ͷ���˲�ͣ����ˮ����ʱ�������� | |
| B�� | ũҵ�����ƹ�ʹ����ࡢ�ι�ȼ��������ˮ���� | |
| C�� | Ϊ���Ϲ�ҵ��ˮ������Ѱ��ˮԴ������ˮ�� | |
| D�� | ֱ�ӽ�������ˮ���뽭���� |
5����ͼ��ʾ�ı仯ֻ�漰�����仯���ǣ�������
| A�� |  ��ľȡ�� | B�� |  ������ˮ | C�� |  ������������ | D�� |  �Ŵ����� |
15����ѧԴ�����������������ϢϢ��أ��������������ѡ����ȷ�����գ�
A��ʯīB������泥�NH4NO3�� C������ D��ʳ��E������أ�KNO3�� F����������
��1����ũ�彨���У������ͥ���������أ���������Ҫ�ɷ���C��
��2����ˮ���þ����ڱڻ����ˮ���������г�ˮ������D��
��3��ũҵ���������Ϸʵ���E��
��4�����A-F��ѡ������±��������ʣ����仯ѧʽ��գ�ÿ��ֻ��һ����ѧʽ����
A��ʯīB������泥�NH4NO3�� C������ D��ʳ��E������أ�KNO3�� F����������
��1����ũ�彨���У������ͥ���������أ���������Ҫ�ɷ���C��
��2����ˮ���þ����ڱڻ����ˮ���������г�ˮ������D��
��3��ũҵ���������Ϸʵ���E��
��4�����A-F��ѡ������±��������ʣ����仯ѧʽ��գ�ÿ��ֻ��һ����ѧʽ����
| ��� | ���� | ������ | �� |
| ��ѧʽ | C | SO2 | KNO3����NH4NO3�� |
2���������ճ������ũҵ�����Ϳ�ѧ�о�����Ӧ�ù㷺��
��1��ijʵ��С��Ϊ��̽��п�����ᷴӦ������Ӱ�����أ�����������ʵ�飮
����ͼ1װ���ռ������������������������Ͳ�����Ǹ��ݽ�����Ͳ��ˮ��������ж��������������������Ӧ��f����e��f��g����ͨ�룮
��Ҫ�Ƚϲ�ͬ��������������Է�Ӧ������Ӱ�죬Ӧѡ���ʵ�����Ǣ٢ۻ�ڢܣ�
���±���С���ڢ���ʵ�����ϸ���ݣ�
������п�����ᷴӦ�Ŀ����ı仯��������Ȼ��������
����ԭ��Ӧ��ʼ�ų��������¶����ߣ���Ӧ�������죬���ŷ�Ӧ�Ľ��У����ᱻ���ģ�������������������С��Ӧ������
��2�����շۣ���ѧʽ Na2S2O4���ڹ�ũҵ�������й㷺����;��Na2S2O4�ڼ�����Һ���ȶ��������Ժ�������Һ�м����ȶ����� NaCl �����£�Na2S2O4��ˮ���ܽ�������½���Na2S2O4�Ʊ�������ͼ2��
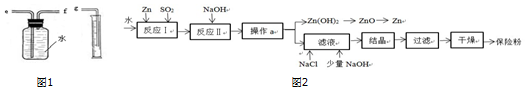
����֪��Ӧ���ԭ��Ϊ��Zn+2SO2�TZnS2O4����Ӧ��Ϊ���ֽⷴӦ����Ӧ��Ļ�ѧ����ʽΪ2NaOH+ZnS2O4�TZn��OH��2��+Na2S2O4��
�ڲ���a������Ϊ���ˣ�
����Һ�к��� Na2S2O4��Ϊʹ Na2S2O4�ᾧ��������Ҫ�������� NaOH ��ԭ����Na2S2O4�ڼ�����Һ���ȶ�������NaCl��ԭ���ǽ��� Na2S2O4��ˮ�е��ܽ�ȣ�
��198gZn��OH��2�������ܵõ�Zn������Ϊ130g��
��1��ijʵ��С��Ϊ��̽��п�����ᷴӦ������Ӱ�����أ�����������ʵ�飮
| ʵ���� | ������������� ����ȡ20mL�� | п����״ ����ȡ1g�� | �����������mL�� �����ռ�3���ӣ� |
| �� | 20% | � | 31.7 |
| �� | 20% | пƬ | 50.9 |
| �� | 30% | � | 61.7 |
| �� | 30% | пƬ | 79.9 |
��Ҫ�Ƚϲ�ͬ��������������Է�Ӧ������Ӱ�죬Ӧѡ���ʵ�����Ǣ٢ۻ�ڢܣ�
���±���С���ڢ���ʵ�����ϸ���ݣ�
| ʱ�Σ���Ϊ1���ӣ� | ��1���� | ��2���� | ��3���� | ��4���� | ��5���� | ��6���� |
| H2����� | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |
����ԭ��Ӧ��ʼ�ų��������¶����ߣ���Ӧ�������죬���ŷ�Ӧ�Ľ��У����ᱻ���ģ�������������������С��Ӧ������
��2�����շۣ���ѧʽ Na2S2O4���ڹ�ũҵ�������й㷺����;��Na2S2O4�ڼ�����Һ���ȶ��������Ժ�������Һ�м����ȶ����� NaCl �����£�Na2S2O4��ˮ���ܽ�������½���Na2S2O4�Ʊ�������ͼ2��

����֪��Ӧ���ԭ��Ϊ��Zn+2SO2�TZnS2O4����Ӧ��Ϊ���ֽⷴӦ����Ӧ��Ļ�ѧ����ʽΪ2NaOH+ZnS2O4�TZn��OH��2��+Na2S2O4��
�ڲ���a������Ϊ���ˣ�
����Һ�к��� Na2S2O4��Ϊʹ Na2S2O4�ᾧ��������Ҫ�������� NaOH ��ԭ����Na2S2O4�ڼ�����Һ���ȶ�������NaCl��ԭ���ǽ��� Na2S2O4��ˮ�е��ܽ�ȣ�
��198gZn��OH��2�������ܵõ�Zn������Ϊ130g��
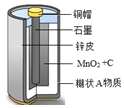 �������ͼ�ش��������⣺
�������ͼ�ش��������⣺