题目内容
13.镁与NH4Cl溶液反应,不仅有一种盐生成,还有气泡产生.为确定生成气体的成分,某化学小组的同学进行了如下实验探究.【查阅资料】①NH3能与水反应生成NH3•H2O;②气体的溶解度随温度的升高而减小;③NH3+HCl═NH4Cl,2NH3+H2SO4═(NH4)2SO4;④NH4Cl溶液和(NH4)2SO4溶液均显酸性.
【提出问题】镁与NH4Cl溶液反应生成何种气体?
【猜想与假设】甲同学说:生成的气体可能是HCl、NH3、H2中的一种或几种.
甲同学提出上述猜想的理论依据是化学反应前后元素种类保持不变.
【进行实验】为了验证以上猜想,小组同学设计了如图装置进行实验:
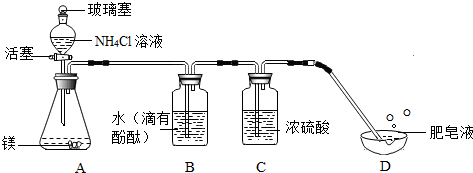
【现象与结论】
| 装置 | 实验现象 | 实验结论 |
| B | 溶液变红 | 生成的气体中含有氨气 |
| D | 肥皂泡飘到空气中,用燃着的木条靠近肥皂泡,有爆鸣声 | 生成的气体中含有 氢气 |
(1)有同学认为不需要单独检验HCl,就能证明HCl不存在,理由是因为氨气能和氯化氢反应生成氯化铵.
(2)C装置中浓硫酸的主要作用是吸收水蒸气和氨气.
(3)写出Mg与NH4Cl溶液反应的化学方程式:Mg+2NH4Cl═MgCl2+2NH3↑+H2↑.
(4)氨气极易溶于水,上述实验中A装置有氨气逸出的原因可能是该反应放热,温度升高,使氨气在水中的溶解度减小.
分析 【猜想与假设】根据质量守恒定律来分析;
【现象与结论】氨水显碱性,能使酚酞试液变红色;氢气密度小,具有可燃性解答;
【反思与评价】
(1)根据氨气能和氯化氢反应生成氯化铵,所以不需要单独检验HCl,就能证明HCl不存在解答;
(2)浓硫酸具有吸水性,能和氨气反应生成硫酸铵;
(3)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式;
(4)根据提供的信息可以判断相关方面的问题.
解答 解:【猜想与假设】由质量守恒定律可知,化学反应前后元素的种类不变,所以猜想可能是HCl、NH3、H2中的一种或几种,故填:化学反应前后元素种类保持不变;
【现象与结论】
B中观察到酚酞试剂变红色,证明产生的气体中有一种能与水反应生成碱性物质,则为氨气,因为氨气与水反应生成氨水,氨水是一种碱,能使无色酚酞试液变红色;
D肥皂泡飘到空气中,用燃着的木条靠近肥皂泡,有爆鸣声,生成的气体中含有氢气;
【反思与评价】
(1)因为氨气能和氯化氢反应生成氯化铵,所以不需要单独检验HCl,就能证明HCl不存在.故填:因为氨气能和氯化氢反应生成氯化铵.
(2)浓硫酸的作用是吸收水蒸气和氨气.
(3)Mg与NH4Cl溶液反应生成MgCl2、NH3和H2,反应的化学方程式为:Mg+2NH4Cl═MgCl2+2NH3↑+H2↑.
(4)氨气极易溶于水,上述实验中A装置有氨气逸出的原因可能是该反应放热,温度升高,使氨气在水中的溶解度减小.
答案:
【猜想与假设】化学反应前后元素种类保持不变;
【现象与结论】
| 装置 | 实验现象 | 实验结论 |
| B | 溶液变红 | 生成的气体中含有氨气 |
| D | 肥皂泡飘到空气中,用燃着的木条靠近肥皂泡,有爆鸣声 | 生成的气体中含有 氢气 |
(1)因为氨气能和氯化氢反应生成氯化铵.
(2)吸收水蒸气和氨气;
(3)Mg+2NH4Cl═MgCl2+2NH3↑+H2↑.
(4)该反应放热,温度升高,使氨气在水中的溶解度减小.
点评 本题是一道实验和结论相结合的题目,可以根据所学知识来回答,难度不大.实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
3.在医疗上葡萄糖C6H12O6被大量用于病人输液,下列关于葡萄糖的说法中不正确的是( )
| A. | 其相对分子质量是180 | B. | 它由C,H,O三种元素组成 | ||
| C. | 它是一种无机物 | D. | 它氧化为生命运动提供能量 |
1.下列说法正确的是( )
| A. | 酸溶液能使紫色石蕊试液变红,所以能使紫色石蕊试液变红的溶液一定是酸 | |
| B. | 所有原子的原子核都是由质子和中子构成 | |
| C. | 含有氧元素的化合物一定是氧化物 | |
| D. | 向NaOH溶液中加水,溶液的pH逐渐变小 |
8.元素周期表是我们学习和研究化学的重要工具,它的内容十分丰富.下面是元素周期表部分内容,请回答下列问题
(1)从表中可查出氧元素的相对原子质量为16.00.
(2)6~11号元素中属于金属元素的有Na(填元素符号).
| 1 H 1.008 | 2 He 4.003 | |||||||
| 3 Li 6.941 | 4 Be 9.012 | … | 5 B 10.81 | 6 C 12.01 | 7 N 14.01 | 8 O 16.00 | 9 F 19.00 | 10 Ne 20.18 |
| 11 Na 22.99 | 12 Mg 24.31 | … | 13 Al 26.98 | 14 Si 28.09 | 15 P 30.97 | 16 S 32.06 | 17 Cl 35.45 | 18 Ar 39.95 |
(2)6~11号元素中属于金属元素的有Na(填元素符号).
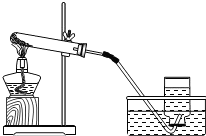 某同学在实验室用以下装置制备氧气并探究氧气的性质.
某同学在实验室用以下装置制备氧气并探究氧气的性质.