题目内容
12.我市每年进行化学实验操作考查,小明在考查实验中出现了下列实验情景,其中操作正确的是( )| A. |  闻气味 | B. | 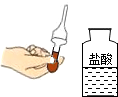 取少量液体 | C. | 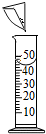 溶解固体 | D. |  滴加试剂 |
分析 A、根据闻气味的正确方法分析;
B、根据胶头滴管的使用方法分析;
C、根据溶解固体操作的方法进行分析;
D、根据胶头滴管的使用方法分析.
解答 解:A、闻气体的气味时,为了防止气体有毒,应用手把瓶口的气体往自己的方向扇动,不能直接用鼻子闻.故A错误;
B、取少量液体时,滴管不能倒置,防止污染滴管胶头,故B错误;
C、溶解固体应在烧杯中进行,不能用量筒溶解固体,故C错误;
D、使用胶头滴管滴加少量液体的操作,注意胶头滴管的位置是不伸入到试管内或接触试管内壁.应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,故D正确.
故选D.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
3.铁暴露在空气中会生锈.不知你注意了没有,将苹果切开不久,果肉上就会产生一层咖啡色的物质,也好象是生了“锈”一样.某化学活动小组对此进行了探究.
【提出问题】切开的苹果“生锈”与什么因素有关?
【猜想与假设】猜想1:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”.
猜想2:可能是果肉中的物质与空气中的氮气作用而“生锈”;
猜想3:可能是果肉中的物质与空气中的氧气作用而“生锈”;
猜想4:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”;
猜想5:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关.
【收集证据】(一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的一种物质发生反应,生成咖啡色的物质.
(二)实验探究:针对上面的猜想1至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次观察到下列实验现象.请你将他们设计的可行的实验探究方案,填写在下表中.
【得出结论】影响切开的苹果“生锈”的因素是空气中的氧气.
【反思与评价】(1)在1~⑤四种猜想中,认为猜想.猜想2最不合理,理由是:氮气的化学性质不活泼.
(2)在验证猜想1时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其可能的原因是溶解在水中的氧气和果肉中的物质发生了反应
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施是隔绝氧气.
【提出问题】切开的苹果“生锈”与什么因素有关?
【猜想与假设】猜想1:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”.
猜想2:可能是果肉中的物质与空气中的氮气作用而“生锈”;
猜想3:可能是果肉中的物质与空气中的氧气作用而“生锈”;
猜想4:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”;
猜想5:可能是果肉中的物质与空气中的氧气作用而“生锈”,并且苹果“生锈”的速度还可能与温度有关.
【收集证据】(一)查阅有关资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的一种物质发生反应,生成咖啡色的物质.
(二)实验探究:针对上面的猜想1至猜想⑤,化学活动小组依次设计了实验方案,进行了实验验证,并依次观察到下列实验现象.请你将他们设计的可行的实验探究方案,填写在下表中.
| 猜想 | 可行的实验方案 | 实验现象 |
| 猜想1 | 将一小块果肉浸入盛有蒸馏水的烧杯中,观察现象. | 果肉表面不变色. |
| 猜想2 | 将一小块切开的苹果放入盛有氮气的集气瓶中,观察现象. | 果肉表面不变色. |
| 猜想3 | 将切开的苹果放入盛有氧气的集气瓶中,观察现象. | 果肉表面变色. |
| 猜想4 | 果肉表面不变色. | |
| 猜想⑤ | 温度高的先变色. |
【反思与评价】(1)在1~⑤四种猜想中,认为猜想.猜想2最不合理,理由是:氮气的化学性质不活泼.
(2)在验证猜想1时,同学们发现,如果水不与空气隔绝,果肉放在水中时间长了也会变色,其可能的原因是溶解在水中的氧气和果肉中的物质发生了反应
【应用】根据上述结论,要防止果汁变质,果品加工厂加工和保存果汁时可采取的措施是隔绝氧气.
20.表为小刘同学研究钢铁生锈的实验报告,请协助该同学分析实验结论:
| 实验编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验条件 | 铁钉放在用水浸湿的棉花球上 | 铁钉浸入迅速冷却的沸水中,塞紧橡皮塞 | 试管内放干燥剂在一团干棉花球上放铁钉,塞紧橡皮绳 |
| 实验图示 | 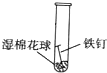 | 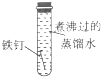 | 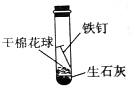 |
| 一周后的实验现象 | 铁钉表面明显生锈 | 铁钉表面无明显锈痕 | 铁钉表面无明显锈痕 |
| 实验结论分析 | ①比较实验Ⅰ、Ⅱ可得出的结论是钢铁生锈需要氧气; ②比较实验Ⅰ、Ⅲ可得出的结论是钢铁生锈需要水 | ||
17.“绿色化学”特点之一是充分利用能源,减少废物向环境排放.下列实验符合“绿色化学“的是( )
| A. | 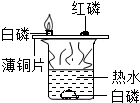 探究燃烧条件 探究燃烧条件 | B. | 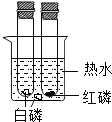 探究燃烧条件 | C. | 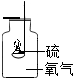 硫燃烧 | D. | 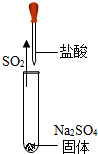 制取少量SO2 |
4.如图反映了某个化学反应各物质质量与时间的关系.下列描述正确的是( )

| A. | 该反应是化合反应 | B. | 甲的相对分子质量大于乙 | ||
| C. | 丙是反应物,甲和乙是生成物 | D. | t1时,表示该反应已经停止 |
3.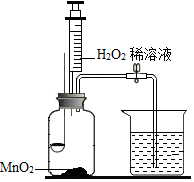 用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃.
用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃.
(1)H2O2溶液于MnO2接触时发生反应的符号表达式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
(2)【实验1】中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,推入H2O2溶液后,观察到燃烧匙中的白磷没有燃烧,烧杯中的现象是导管口有气泡冒出,且白磷燃烧.
(3)【实验2】中,推入H2O2溶液后,观察到木炭燃烧的更剧烈,由此得出氧气的性质是助燃性;木炭熄灭后冷却一段时间,烧杯中的部分澄清石灰水溶液流入集气瓶中并变浑浊,该实验中,说明木炭在氧气中燃烧的生成物是二氧化碳.
 用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃.
用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验,已知:白磷的着火点为40℃.| 内容 | 【实验1】研究燃烧条件 | 【实验2】研究氧气性质 |
| 步骤1 | 烧杯中盛有80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞. | 烧杯中盛有澄清的石灰水,燃烧匙中放入木炭,点燃木炭后,迅速将燃烧匙伸入瓶中,塞紧瓶塞. |
| 步骤2 | 推入适量H2O2溶液 | 推入适量H2O2溶液 |
(2)【实验1】中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,推入H2O2溶液后,观察到燃烧匙中的白磷没有燃烧,烧杯中的现象是导管口有气泡冒出,且白磷燃烧.
(3)【实验2】中,推入H2O2溶液后,观察到木炭燃烧的更剧烈,由此得出氧气的性质是助燃性;木炭熄灭后冷却一段时间,烧杯中的部分澄清石灰水溶液流入集气瓶中并变浑浊,该实验中,说明木炭在氧气中燃烧的生成物是二氧化碳.