题目内容
18.新版《生活饮用水卫生标准》中水质检测指标从原来的35项增加到106项,对供水各环节的水质提出了相应的要求.(1)新国标在无机物指标中修订了镉、铅等的限量.这里的镉、铅指的是C(填序号).
A.原子 B.分子 C.元素 D.单质
(2)新国标中对水的pH规定为6.5≤pH≤8.5.实验室用pH试纸测得自来水的pH=8,说明该自来水显酸(填“酸”、“碱”或“中”)性.
(3)新国标中消毒剂由1项增至4项,加入了对用臭氧、二氧化氯和氯胺消毒的规定.
①臭氧(O3)在消毒过程中转化为氧气,该过程发生的是化学(填“物理”或者“化学”)变化.
②二氧化氯消毒过程中产生的次氯酸根(ClO-)也有消毒作用,ClO-中氯元素的化合价为+1.
③用氯胺(NH2Cl)消毒,反应的化学方程式为NH2Cl+X=NH3+HClO,其中X的化学式为H2O.
分析 根据物质是由元素组成的、溶液的酸碱性与pH的关系、化学变化时有新物质生成、离子中各元素的化合价之和等于离子的化合价、以及化学反应前后元素的种类和原子的个数不变进行确定物质的化学式即可.
解答 解:(1)物质是由元素组成的,故这里的镉、铅指的是元素,故填:C;
(2)实验室用pH试纸测得自来水的pH=6,pH小于7的溶液呈酸性,故说明该自来水显酸性,故填:酸;
(3)①臭氧(O3)在消毒过程中转化为氧气,生成了新的物质,故臭氧转化为氧气属于化学变化,故填:化学;
②ClO-的化合价为-1,氧元素的化合价为-2,设氯元素的化合价为x,则有x+(-2)=-1,故x=+1,故填:+1;
③由于化学反应前后各原子的种类和个数不变,依据反应的化学方程式NH2Cl+X═NH3+HClO,反应前含有1个N原子,2个H原子,1个Cl原子和X,反应后含有1个N原子,4个H原子,1个Cl原子,1个O原子,故X中含有2个H原子和1个O原子,故其化学式为H2O,故填:H2O.
点评 本题考查的是物质的组成和质量守恒的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
9.了解安全知识,可以更好地保护人身和财产安全.下列做法不正确的是( )
| A. | 炒菜时油锅着火,可立即加水灭火 | |
| B. | 发现煤气泄漏应立即关阀门开窗通风 | |
| C. | 不要用湿手接触带电体,以免发生触电危险 | |
| D. | 不能用甲醛浸泡食品进行保鲜 |
3.我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如下所示),反应原理为NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3(析出),促进了世界制碱技术的发展.下列说法正确的是( )
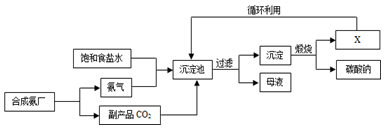

| A. | 沉淀池中的反应物共含有4种元素 | |
| B. | 通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 | |
| C. | 图中X可能是氨气 | |
| D. | 过滤得到的“母液”中一定只含有两种溶质 |
10.甲同学在生活中处处注意观察,他发现固体在水中的溶解快慢受很多因素的影响,于是他进行了下表所示的实验.请你参与探究并填空:
【探究课题】影响硝酸钾固体在水中溶解快慢的因素有哪些?
【实验假设】1.温度; 2.搅拌;3.颗粒大小
【探究准备】烧杯、铁架台、托盘天平、酒精灯、玻璃棒、量筒、药匙、石棉网、颗粒大小不同的硝酸钾固体、蒸馏水.
【探究过程】
【探究结论】通过上述探究得出结论:影响硝酸钾固体在水中溶解快慢的因素有温度、搅拌、颗粒大小.
【探究应用】如何使方糖比较快的溶解在水中?要使方糖较快地溶解在水中,可以将研成粉末状、放入热水中并用玻璃棒搅拌.
【探究课题】影响硝酸钾固体在水中溶解快慢的因素有哪些?
【实验假设】1.温度; 2.搅拌;3.颗粒大小
【探究准备】烧杯、铁架台、托盘天平、酒精灯、玻璃棒、量筒、药匙、石棉网、颗粒大小不同的硝酸钾固体、蒸馏水.
【探究过程】
| 探究内容 | 探究方法 | 探究现象 |
| 温度 对硝酸钾固体溶解快慢的影响 | ①取两个烧杯,分别加入l0mL等温的水 ②再分别加入l g同样颗粒大小的硝酸钾固体 ③给其中一个烧杯加热 | 被加热的烧杯里的硝酸钾固体完全溶解用得时间短 |
| 搅拌对硝酸钾固体溶解快慢的影响 | ①取两个烧杯,分别加入l0mL等温的水 ②再分别加入l g同样颗粒大小的硝酸钾固体 ③搅拌其中一个烧杯里的硝酸钾固体 | 搅拌的烧杯里的硝酸钾固体完全溶解用得时间短 |
| 颗粒大小对硝酸钾固体溶解快慢的影响 | ①取两个烧杯,分别加入l0mL等温的水 ②向其中一个烧杯加入l g颗粒大的硝酸钾固体,向另一个烧杯加入l g粉末状的硝酸钾固体 | 颗粒小的硝酸钾固体完全溶解用得时间短 |
【探究应用】如何使方糖比较快的溶解在水中?要使方糖较快地溶解在水中,可以将研成粉末状、放入热水中并用玻璃棒搅拌.
8.兴趣小组同学发现实验台上整齐摆放的药品中(见图),有一试剂瓶的标签破损.
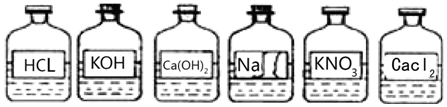
【提出问题】这瓶试剂的成分是什么?
【讨论】根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是A.
A.酸 B.碱 C.盐
【猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl溶液
【设计并实验】
(1)小明用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,于是他判断这是NaOH溶液.对他的操作方法、测量结果及结论的评价,正确的是B.
A.操作方法正确,结果正确,且结论正确
B.操作方法正确,结果偏小,且结论也不正确
C.操作方法不正确,结果偏大,结论不正确
D.操作方法不正确,结果正确,但结论不正确
根据实验数据,你认为一定不可能是哪个猜想(填序号),并简单阐述你的依据③,氯化钠的水溶液呈中性.
(2)要进一步确定它的成分,小俊认为只需选择上图已有的试剂就能把它鉴别出来,他们又进行了实验,并且得到了正确的结果.请填写完成下表:
(3)小强认为还有可能是另一种溶液,请你写出溶质的化学式NaOH.

【提出问题】这瓶试剂的成分是什么?
【讨论】根据受损标签及实验室药品分类摆放的原则,这瓶试剂不可能是A.
A.酸 B.碱 C.盐
【猜想】①可能是NaOH溶液;②可能是Na2CO3溶液;③可能是NaCl溶液
【设计并实验】
(1)小明用洁净干燥的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=10,于是他判断这是NaOH溶液.对他的操作方法、测量结果及结论的评价,正确的是B.
A.操作方法正确,结果正确,且结论正确
B.操作方法正确,结果偏小,且结论也不正确
C.操作方法不正确,结果偏大,结论不正确
D.操作方法不正确,结果正确,但结论不正确
根据实验数据,你认为一定不可能是哪个猜想(填序号),并简单阐述你的依据③,氯化钠的水溶液呈中性.
(2)要进一步确定它的成分,小俊认为只需选择上图已有的试剂就能把它鉴别出来,他们又进行了实验,并且得到了正确的结果.请填写完成下表:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样品于试管中,加入 足量的稀盐酸 | 猜想②正确;相关的化学反应方程式: Na2CO3+2HCl═2NaCl+H2O+CO2↑ |

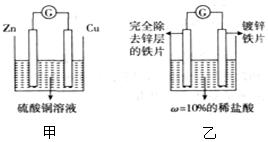
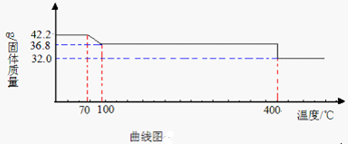
 如图所示是晓星将一定质量的铁铁粉加入到100g稀硫酸溶液中,反应进行的时间和产生的气体的质量之间的关系图象.求:(忽略气体溶解度)
如图所示是晓星将一定质量的铁铁粉加入到100g稀硫酸溶液中,反应进行的时间和产生的气体的质量之间的关系图象.求:(忽略气体溶解度)