题目内容
4. 砝码是化学实验室中的常用实验器材,如图所示是一盒砝码的实物图,请你回答下列问题:
砝码是化学实验室中的常用实验器材,如图所示是一盒砝码的实物图,请你回答下列问题:(1)不锈钢属于混合物(填“单质”、“化合物”或“混合物”)图中属于合成材料的是塑料.
(2)砝码表面镀铬不仅美观,还可以防止砝码生锈.
(3)铬能缓慢溶解于稀盐酸和稀硫酸,由此推测铬的金属活动性比较强,铬在浓硫酸中发生反应的化学方程式为:2Cr+6H2SO4(浓)═Cr2(SO4)3+3SO2↑+6H2O,产生的SO2可用碱性(填“酸”或“碱”)溶液来吸收,以减少对环境的污染.
分析 (1)根据合金属于混合物解答;根据有机合成材料是指人工利用有机高分子化合物制成的材料,主要包括塑料、合成纤维、合成橡胶等,据此分析解答即可;
(2)根据防止生锈的条件解答;
(3)根据在金属活动性顺序中,氢前的金属能与酸反应生成氢气,由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
解答 解:(1)不锈钢是合金,属于混合物;图中属于合成材料的是塑料;
(2)砝码表面镀铬不仅美观,还可以防止砝码生锈;
(3)在金属活动性顺序中,氢前的金属能与酸反应生成氢气,铬能缓慢溶解于稀盐酸和稀硫酸,由此推测铬的金属活动性比较强;
由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2Cr+6H2SO4(浓)═_______+3SO2↑+6H2O,
反应前铬、氢、硫、氧原子个数分别为2、12、6、24,反应后的生成物中铬、氢、硫、氧原子个数分别为0、12、3、12,根据反应前后原子种类、数目不变,则每个分子由2个铬原子、3个硫原子和12个氧原子构成,则物质的化学式为Cr2(SO4)3;产生的SO2可用氢氧化钠溶液来吸收,以减少对环境的污染.
答案:
(1)混合物;塑料;
(2)防止砝码生锈;
(3)强;Cr2(SO4)3;碱.
点评 此题考查各种金属的物理性质和金属活动性顺序表.此题很简单,已在考察基础知识的运用.学生应熟悉物质的性质及物质之间的反应来解答.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
14.掌握化学用语是学习化学的关键,请用化学用语填空:
(1)硫离子S2-;(2)2个汞原子2Hg;(3)氨气中氮的化合价$\stackrel{-3}{N}$H3;(4)保持氢气化学性质的最小微粒H2.
(1)硫离子S2-;(2)2个汞原子2Hg;(3)氨气中氮的化合价$\stackrel{-3}{N}$H3;(4)保持氢气化学性质的最小微粒H2.
15.下列实验设计,不能达到实验目的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 鉴别涤纶面料与羊毛面料 | 取样后,分别灼烧,闻气味 |
| B | 食盐溶液和盐酸 | 取样后,滴加无色酚酞试液 |
| C | 鉴别碳粉和氧化铜粉末 | 取样后,分别加入稀硫酸,加热 |
| D | 区分硝酸铵粉末和氧化钙粉末 | 取样后,分别加水 |
| A. | A | B. | B | C. | C | D. | D |
19.推理是一种重要的学习方法,下列推理正确的是( )
| A. | 磁感线既表示了磁场的分布,也表示了磁场的方向 | |
| B. | 水是由分子组成的,所以一切物质都是由分子组成 | |
| C. | 元素符号表示某种元素,所以不能表示某元素的原子 | |
| D. | 植物接受光照进行光合作用,所以不会进行呼吸作用 |
9.为了测定某黄铜(铜锌合金)样品的组成,某化学兴趣小组的同学进行了以下实验:取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入硫酸,充分反应后用天平称量,记录实验数据如表:
请回答下列问题并计算:
(1)经分析,在第1次实验结束后,反应物稀硫酸完全反应完了.
(2)50.0g样品与足量稀硫酸反应最多能生成气体0.5g
(3)计算样品中锌的质量分数(写出具体计算过程).
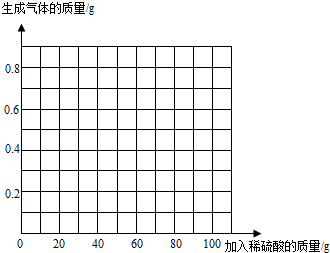
(4)请在图中画出加入稀硫酸的质量与生成气体的质量的变化关系.
| 试验次序 | 第1次 | 第2次 | 第3次 | 第4次 |
| 所取样品的质量 /g | 50.0 | 50.0 | 50.0 | 50.0 |
| 加入稀硫酸的质量/g | 20.0 | 40.0 | 60.0 | 80.0 |
| 生成气体的质量/g | 0.2 | 0.4 | 0.5 | 0.5 |
(1)经分析,在第1次实验结束后,反应物稀硫酸完全反应完了.
(2)50.0g样品与足量稀硫酸反应最多能生成气体0.5g
(3)计算样品中锌的质量分数(写出具体计算过程).
(4)请在图中画出加入稀硫酸的质量与生成气体的质量的变化关系.

16.防治污染、改善环境已成为人们的共识.下列措施中,不利于改善大气质量、保护环境的是( )
| A. | 城市主干道洒水保洁 | B. | 使用电动汽车使生活更加便捷 | ||
| C. | 提倡使用太阳能热水器 | D. | 丰收后焚烧作物秸秆为天地施肥 |