题目内容
同学们在实验室用5%的H2O2溶液制取氧气并进行氧气性质实验.
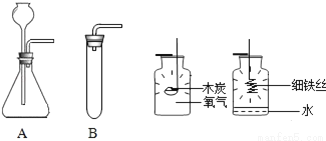
溶液配制:用50g30%的H2O2溶液(密度为1.13/cm3)配制5%的H2O2溶液(密度约为1g/cm3).溶液配制过程中,除用到玻璃棒外,还需用到下列仪器中的__.
A、托盘天平 B、烧杯 C、漏斗 D、量筒 E、胶头滴管
气体制备:用配制好的5%H2O2溶液和MnO2制取O2.请你在“A”、“B”两套装置中选择其中一套,并说明选择的理由_____(合理即可),该反应的化学方程式为___.待反应结束后同学们回收了混合物中的MnO2,实验操作为_____
性质实验:小明用收集好的氧气,进行了下面的实验:
把点燃的木条伸入集气瓶中,实验现象是______;为使铁丝在氧气中持续燃烧,他把光亮的细铁丝盘成螺旋状 _________,缓慢插入集气瓶中,观察到的现象是________.通过实验得出,氧气可以支持燃烧,并且可燃物燃烧更剧烈.
BDE A便于添加液体药品或B装置简单,节约药品(合理即可) 2H2O22H2O+O2 过滤、干燥 发出白光,放出热量 下端系一根火柴,点燃火柴待火柴快燃尽时 剧烈燃烧火星四射放出热量生成黑色固体 【解析】(1)溶液配制:用50g30%的H2O2溶液(密度为1.13/cm3)配制5%的H2O2溶液(密度约为1g/cm3),步骤为;计算、量取、溶解,因此需要的仪器有:量筒、胶头滴管、烧杯、玻璃...
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
对下列事实解释错误的是( )
选项 | 事 实 | 解 释 |
A | 氧气加压可变成液氧 | 加压可使分子体积变小 |
B | 金刚石很硬,石墨质软 | 碳原子排列方式不同 |
C | 过氧化氢溶液是混合物 | 由不同种分子构成 |
D | 宝石绚丽多彩 | 宝石中含有某些金属离子 |
A. A B. B C. C D. D
A 【解析】A、氧气加压后变成液氧,分子的体积没变,分子之间的间隙变大,错误; B、由于金刚石和石墨的碳原子排列方式不同,故物理性质不同,正确; C、过氧化氢溶液是由不同的分子构成,故是混合物,正确; D、宝石中含有某些金属离子,故宝石中含有某些金属离子,正确。故选A。


 Fe(OH)2
Fe(OH)2 Fe(OH)3
Fe(OH)3 Fe2O3•xH2O
Fe2O3•xH2O