题目内容
4.根据如图所示实验过程和提供的数据计算:
(1)反应生成氧气的质量为1.6g.
(2)计算过氧化氢中溶质的质量分数.
分析 过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应前后的质量差即为反应生成氧气的质量,根据氧气质量可以计算过氧化氢质量,进一步可以计算过氧化氢中溶质的质量分数.
解答 解:(1)反应生成氧气的质量为:1.0g+80.0g-79.4g=1.6g.
故填:1.6.
(2)设过氧化氢质量为x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
68 32
x 1.6g
$\frac{68}{x}$=$\frac{32}{1.6g}$,
x=3.4g,
过氧化氢中溶质的质量分数为:$\frac{3.4g}{80.0g}$×100%=4.25%,
答:过氧化氢中溶质的质量分数为4.25%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
相关题目
14.下列变化过程中,构成物质的分子分裂成原子,原子又重新组合成其它物质分子的是( )
| A. | 给水通电分解 | B. | 活性炭吸附有毒气体 | ||
| C. | 铁钉放入硫酸铜溶液中 | D. | 氢氧化钠溶液中滴入氯化铁溶液 |
15.下列富含蛋白质的食物是( )
| A. |  水果 | B. |  蔬菜 | C. |  肉类 | D. |  油 |
13.下列化学用语中,正确的是( )
| A. | n个蔗糖分子:(C12H22O)n | B. | 镁元素的化合价为“+2”价:$\stackrel{+2}{Mg}$ | ||
| C. | 氧化钠:NaO | D. | 3个铁离子:3Fe2+ |
14.根据图中的信息判断,下列说法错误的是( )


| A. | 硫原子的质子数是16 | |
| B. | 硫原子核外有3个电子层 | |
| C. | 当x=8时,该微粒是S2- | |
| D. | 该元素为非金属元素,其原子在化学变化中易失去电子 |
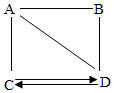 A、B、C、D为初中化学常见不同类别的物质,他们之间的反应关系如图所示(“→”表示转化关系,“-”表示相互能反应,部分反应物、生成物已略去).A是胃液的主要成分,D常用于改良酸性土壤,A→C的反应后溶液为黄色.请回答:
A、B、C、D为初中化学常见不同类别的物质,他们之间的反应关系如图所示(“→”表示转化关系,“-”表示相互能反应,部分反应物、生成物已略去).A是胃液的主要成分,D常用于改良酸性土壤,A→C的反应后溶液为黄色.请回答: 某同学在实验室用高锰酸钾制取氧气的实验中,其固体的质量M与之间T的关系如图所示,回答下列问题:
某同学在实验室用高锰酸钾制取氧气的实验中,其固体的质量M与之间T的关系如图所示,回答下列问题: