题目内容
19.将一小块银白色的金属钠放置在空气中会发生下列变化:钠(Na)$\stackrel{O_{2}}{→}$钠的氧化物$\stackrel{H_{2}O}{→}$氢氧化钠溶液$\stackrel{CO_{2}}{→}$白色固体
[提出问题]
常温下钠与氧气反应,产物有哪些?
[查阅资料]
钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠和过氧化钠都能与水发生反应,方程式如下:Na2O+H2O═2NaOH;2Na2O2+2H2O═4NaOH+O2↑
[作出猜想]
常温下钠与氧气反应的产物.
猜想1:Na2O;
猜想2:Na2O2;
猜想3:Na2O和Na2O2.
[实验探究一]
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 没有气泡生成 | 猜想1正确 |
[作出猜想]
猜想一:Na2CO3,
猜想二,Na2CO3和NaOH
[实验探究二]
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量氯化钙溶液 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2.过滤,取少量滤液加入无色的酚酞试液 | 变成红色 |
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式Na2O+2HCl=2NaCl+H2O.
(2)过氧化钠也能与盐酸反应,方程式为2Na2O2+4HCl═4NaCl+2H2O+X↑,X的化学式为O2.
分析 【作出猜想】根据钠与氧气反应的产物进行猜想;
【实验探究一】:根据氧化钠与水反应的现象分析;
【实验探究二】:根据碳酸钠、氢氧化钠的性质、检验方法分析回答;
【实验反思】(1)根据氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式;
(2)根据质量守恒定律分析X的化学式;
解答 解:【作出猜想】由于钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),所以猜想三是:Na2O和Na2O2;
【实验探究一】:由于氧化钠与水反应生成了氢氧化钠,所以,取少量钠的氧化物加入足量蒸馏水,现象是没有气泡生成,证明猜想一正确;
【实验探究二】:由于碳酸钠与足量的氯化钙反应生成了碳酸钙和氯化钠,溶液呈中性,氢氧化钠能使酚酞试液变红色.所以.填表如下:
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量 氯化钙溶液 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2.过滤,取少量滤液加入 无色的酚酞试液 | 变成红色 |
【实验反思】(1)由氧化铜与盐酸的反应生成了氯化铜和水可知,氧化钠与盐酸反应生成了氯化钠和水,化学方程式是:Na2O+2HCl=2NaCl+H2O;
(2)由质量守恒定律反应后原子的种类及数目不变可知,方程式得到右边还缺少两个氧原子,所以,分析X的化学式是:O2.
故答案为:【作出猜想】Na2O和Na2O2;
【实验探究一】:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量钠的氧化物加入足量蒸馏水 | 没有气泡生成 | 猜想1正确 |
| 实验操作 | 实验现象 | 实验结论 |
| 1.取少量白色固体加入足量 氯化钙溶液 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
| 2.过滤,取少量滤液加入 无色的酚酞试液 | 变成红色 |
【实验反思】(1)Na2O+2HCl=2NaCl+H2O;(2)O2.
点评 该题根据查阅资料提供的信息并结合实验步骤和现象解决问题.主要考查读题能力,能把题目所给信息与所学知识进行牵连.知道性质决定用途,用途体现性质.

练习册系列答案
相关题目
9.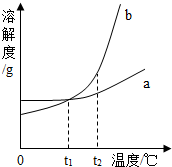 如图是a、b两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )
如图是a、b两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )
 如图是a、b两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )
如图是a、b两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是( )| A. | t2℃时,a溶液的溶质质量分数一定小于b溶液的溶质质量分数 | |
| B. | t1℃时,a、b两种物质的饱和溶液溶质质量分数相同 | |
| C. | 将t2℃时b的不饱和溶液降温至t1℃,一定能得到b的饱和溶液 | |
| D. | 若a中混有少量的b,可以用降温结晶的方法提纯a |
8.黄金溶解在“王水”(浓盐酸与浓硝酸的混合液)中形成HAuCl4(四氯合金酸),没有氢气产生.根据以上信息,下列有关说法正确的是( )
①“王水”溶解黄金是化学变化;②金比氢活泼;③HAuCl4中,Au的化合价为+3价;
④可以将pH试纸伸入“王水”中测其酸碱度;⑤“王水”可以用铁质容器盛装.
①“王水”溶解黄金是化学变化;②金比氢活泼;③HAuCl4中,Au的化合价为+3价;
④可以将pH试纸伸入“王水”中测其酸碱度;⑤“王水”可以用铁质容器盛装.
| A. | ①④⑤ | B. | ①②③ | C. | ③④⑤ | D. | ①③ |
9.如图为甲乙两种固体在水中的溶解度曲线,下列说法正确的是( )
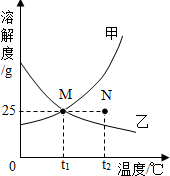

| A. | t2时,将甲乙两种物质的饱和溶液降低至t1,仍为饱和溶液 | |
| B. | t1时,甲乙饱和溶液的溶质质量分数为20% | |
| C. | 甲物质中混有少量乙,可采用蒸发溶剂方法提纯甲 | |
| D. | t2时,N点表示乙物质的不饱和溶液 |