题目内容
6.下列关于化学反应的实验现象描述正确的是( )| A. | 打开盛有浓盐酸的试剂瓶,看到瓶口有大量白雾 | |
| B. | 在电解水实验中,正负两极产生的气体体积比约为2:1 | |
| C. | 木炭在空气中燃烧生成黑色有刺激性气味的气体 | |
| D. | 铁丝在氧气中剧烈燃烧,火星四射,放出大量热,生成四氧化三铁 |
分析 A、根据浓盐酸的性质解答;
B、根据电解水时正氧负氢、氢二氧一解答;
C、根据木炭燃烧的现象解答;
D、根据铁丝在氧气中燃烧的实验现象解答.
解答 解:A、打开盛有浓盐酸的试剂瓶,看到瓶口有大量白雾,正确;
B、在电解水实验中,正负两极产生的气体体积比约为2:1,是实验的结论,不是实验的现象,错误;
C、炭在空气中燃烧生成无色无味的气体,错误;
D、铁丝在氧气中剧烈燃烧,火星四射,放出大量热,生成四氧化三铁属于实验的结论不是实验的现象,错误;
故选A.
点评 本题考查的是常见的实验现象的描述,完成此题,可以依据已有的知识进行,要注意实验现象和实验结论的区别.

练习册系列答案
相关题目
14.一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量见表,下列税说法正确的是( )
| 物质 | a | b | c | d |
| 反应前物质质量/g | 18 | 1 | 2 | 32 |
| 反应后物质质量/g | 待测 | 26 | 2 | 12 |
| A. | 待测数据是23 | B. | 参加反应a、d的质量比为4:1 | ||
| C. | 该反应的基本类型为化合反应 | D. | c物质一定是该反应的催化剂 |
1.下列说法正确的是( )
| A. | 一氧化碳在空气中燃烧产生蓝色火焰 | |
| B. | 木炭燃烧后生成白色固体 | |
| C. | 红磷在空气中燃烧产生大量白雾 | |
| D. | 硫在氧气中燃烧产生淡蓝色火焰 |
11.如图所示,某化学兴趣小组用H2O2溶液MnO2制取干燥的氧气,并用来测定10g某铜粉样品(含杂质碳)中铜的质量分数.回答下列问题:
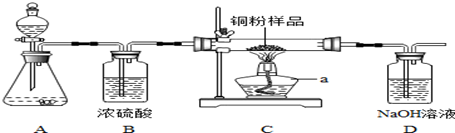
(1)装置A中发生反应的化学方程式是2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.装置B的作用是干燥氧气.
(2)通过称量反应前后装置D的质量,进行计算便可求出样品中铜的质量分数.
(3)实验完毕,小丽误将用剩的H2O2溶液和装置C中的剩余固体一起倒入烧杯中,发现有大量的气泡产生,经检验产生的气体是氧气.小刚和小明对此颇感兴趣,展开了他们的探究之旅.
【提出问题】是哪种物质加快了H2O2的分解速率?
【大胆猜想】猜想Ⅰ:剩余固体中的CuO加快了H2O2溶液的分解.猜想Ⅱ:剩余固体中的铜加快了H2O2溶液的分解.
【实验验证】

(1)装置A中发生反应的化学方程式是2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.装置B的作用是干燥氧气.
(2)通过称量反应前后装置D的质量,进行计算便可求出样品中铜的质量分数.
(3)实验完毕,小丽误将用剩的H2O2溶液和装置C中的剩余固体一起倒入烧杯中,发现有大量的气泡产生,经检验产生的气体是氧气.小刚和小明对此颇感兴趣,展开了他们的探究之旅.
【提出问题】是哪种物质加快了H2O2的分解速率?
【大胆猜想】猜想Ⅰ:剩余固体中的CuO加快了H2O2溶液的分解.猜想Ⅱ:剩余固体中的铜加快了H2O2溶液的分解.
【实验验证】
| 实验方案 | 实验现象 | 分析及结论 |
| 实验一:将带火星的木条伸入盛有5mL5%H2O2溶液的试管 | 带火星木条不复燃 | H2O2溶液常温下产生氧气缓慢,不足以使带火星的木条复燃 |
| 实验二:向盛有5mL5%H2O2溶液的试管中加入1gCuO固体,将带火星的木条伸入试管,观察现象.待反应结束后将试管里的剩余物进行过滤、洗涤、干燥、称量.对比反应前后CuO的质量 | 带火星的木条复燃. 称得固体质量为1g | 猜想Ⅰ成立.反应前后氧化铜的质量相等 |
| 实验三:向盛有5mL5%H2O2溶液的试管中加入1g铜,将带火星的木条伸入试管,观察现象 | 没有气泡产生,带火星木条不复燃 | 猜想Ⅱ不成立(填”成立“或“不成立”) |
18.“类推”是化学学习过程中常用的思维方法,现有以下类推结果,其中正确的是( )
| A. | 因为碱溶液呈碱性,所以呈碱性的溶液一定是碱溶液 | |
| B. | 金属铝与盐酸反应生产AlCl3和H2,所以金属铁与盐酸反应生产FeCl3和H2 | |
| C. | 中和反应一定能生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| D. | 因为甲烷燃烧生成二氧化碳和水,所以甲烷中一定含有碳元素和氢元素 |
15.下列有关溶液的叙述中正确的是( )
| A. | 一种溶液中只能含一种溶质 | |
| B. | 95ml酒精和5ml水混合后溶剂是酒精 | |
| C. | 溶液是一种均一、稳定的混合物 | |
| D. | 溶液中的溶成质一定是固体,溶剂一定是水 |
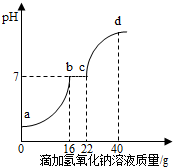 为测定某工业盐酸中氯化铁的含量(假设工业盐酸中不含其它杂质),小娟做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为20%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如右图所示的关系.
为测定某工业盐酸中氯化铁的含量(假设工业盐酸中不含其它杂质),小娟做了如下实验:取20g工业盐酸加入到小烧杯中,然后向小烧杯中不断滴加溶质质量分数为20%的氢氧化钠溶液,同时用电子pH计不断读取反应时的pH,得出如右图所示的关系.