题目内容
7. 某同学在做“硫在氧气中燃烧”的实验时,为了防止空气污染,用氢氧化钠溶液来吸收二氧化硫.下面是该同学实验与计算过程:
某同学在做“硫在氧气中燃烧”的实验时,为了防止空气污染,用氢氧化钠溶液来吸收二氧化硫.下面是该同学实验与计算过程:(1)配制50g溶质质量分数为5%的氢氧化钠溶液.
①需用天平称取2.5g的氢氧化钠;
②配制上述溶液,可用10%氢氧化钠溶液25g加水稀释.
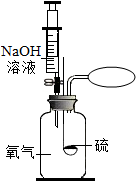
(2)如图所示,硫燃烧后,注入所配制的NaOH溶液吸收二氧化硫.若集气瓶中生成0.32g的二氧化硫,将其完全吸收,针筒要吸取的氢氧化钠溶液中含氢氧化钠多少克?.(假设NaOH溶液吸收SO2时只发生如下反应:SO2+2NaOH=Na2SO3+H2O)
分析 溶液稀释前后溶质质量不变;
根据提供的数据可以进行相关方面的计算.
解答 解:(1)①需要氢氧化钠的质量为:50g×5%=2.5g;
②设需要氢氧化钠溶液的质量为x,
x×10%=2.5g,
x=25g.
故填:2.5;25g.
(2)解:设含有氢氧化钠的质量为y,
SO2+2NaOH=Na2SO3+H2O,
64 80
0.32g y
$\frac{64}{0.32g}$=$\frac{80}{y}$,
y=0.4g,
答:含有0.4g氢氧化钠.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
16.生活中的下列物质属于溶液的是( )
| A. | 牛奶 | B. | 糖水 | C. | 石灰乳 | D. | 泥浆水 |
1.下列药品中,不需要密封保存的是( )
| A. | 石灰石 | B. | 浓硫酸 | C. | 氢氧化钠 | D. | 生石灰 |
 A、B、C三种物质的溶解度曲线,试回答:
A、B、C三种物质的溶解度曲线,试回答: