题目内容
14.如图所示是空气的自述,你认为在它对自己的认识中,不正确的有(已知氮元素的原子序数为7)
| A. | 1处 | B. | 2处 | C. | 3处 | D. | 4处 |
分析 根据空气的成分以及各成分的体积分数、性质等分析判断;原子序数=质子数.
解答 解:由空气的自述可知:
①空气含有氮气、氧气等物质,属于混合物不属于纯净物;
②空气中含有氮分子、氧分子等,不含有空气分子;
③氮气的质子数无法确定,因为不知道有多少个氮分子;
④空气中氧气的体积分数约为$\frac{1}{5}$.
由以上分析可知由4处错误.
故选D.
点评 本题较为简单,了解空气的成分以及各成分的体积分数、性质等知识即可分析判断.

练习册系列答案
相关题目
14. 化学大厦里的“居民”们(即各种物质)按各自所属的类别分类居住在A、B两座大楼里.如表是已经入住的“居民”的情况:
化学大厦里的“居民”们(即各种物质)按各自所属的类别分类居住在A、B两座大楼里.如表是已经入住的“居民”的情况:
(1)化学大厦来了一位新“居民”--NaHCO3,他应该住进六单元.大厦中有一位“居民”住错了地方,它是Na2CO3.
(2)三单元中CO2和CO组成相同,但性质差别很大,原因是分子构成不同.
(3)六单元里住着一位“制氧高手”,写出实验室由它制取氧气的化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
 化学大厦里的“居民”们(即各种物质)按各自所属的类别分类居住在A、B两座大楼里.如表是已经入住的“居民”的情况:
化学大厦里的“居民”们(即各种物质)按各自所属的类别分类居住在A、B两座大楼里.如表是已经入住的“居民”的情况:| 化学大厦 | A座 | 一单元 | Mg Al Fe |
| 二单元 | H2 O2 S | ||
| B座 | 三单元 | CO2 CO SO2 | |
| 四单元 | Ca(OH)2 KOH Na2CO3 | ||
| 五单元 | H2SO4 HNO3 HCl | ||
| 六单元 | KMnO4 FeCl2 CuSO4 |
(2)三单元中CO2和CO组成相同,但性质差别很大,原因是分子构成不同.
(3)六单元里住着一位“制氧高手”,写出实验室由它制取氧气的化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
15.下列说法正确的是( )
| A. | 盐的组成中不一定含有金属离子 | B. | 食盐就是盐,盐就是食盐 | ||
| C. | 盐的组成中一定没有氢离子 | D. | 盐的组成中一定没有氢氧根离子 |
2.如图1是化学课外活动小组设计的探究工业炼铁实验原理,其中A装置的作用是将二氧化碳和碳粉在高温下转化为一氧化碳,回答下列问题:
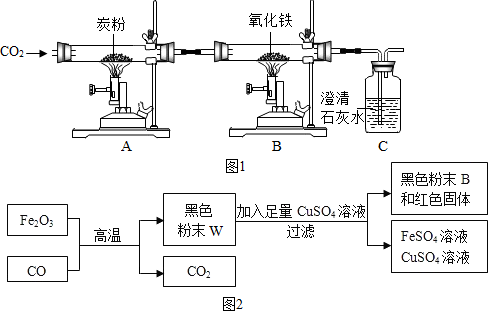
(1)写出装置A玻璃管中发生反应的化学方程式:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO;
(2)整套装置还有一个明显的不足之处是:缺少尾气处理装置.
(3)B中得到的黑色产物W,该活动小组同学根据图2对产物W的成分进行探究.
【提出问题】黑色粉末W可能是什么呢?
【查阅资料】
①铁的氧化物有氧化铁,氧化亚铁和四氧化三铁等,其中氧化铁为红棕色,其余都为黑色.
②铁的氧化物中四氧化三铁有磁性,能被磁铁吸引.
③铁的氧化物都难溶于水,却都能与稀盐酸反应而被溶解.
④铁的氧化物通常情况下不与CuSO4溶液反应.
【进行猜想】
①甲同学认为黑色粉末W全部是铁粉.请写出生成铁的化学反应方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.该反应利用了CO的还原性.
②乙同学认为甲同学的猜想是错误的,理由是黑色粉末W与足量的硫酸铜溶液反应后仍有黑色固体存在.
③丙同学认为黑色粉末W中不含Fe2O3,理由是氧化铁是红棕色的固体.
丙同学提出如下猜想,请你结合所学知识帮他补充完整.
猜想1:黑色粉末W由铁粉和四氧化三铁(Fe2O3)组成;
猜想2:黑色粉末W由铁粉和氧化亚铁(FeO)组成;
猜想3:黑色粉末W由铁粉、四氧化三铁(Fe2O3)、氧化亚铁(FeO).
【实验探究】
【得出结论】在高温下一氧化碳和氧化铁反应可生成铁、氧化亚铁、四氧化三铁.
【反思提高】
丁同学认为方案②和方案③中得出的结论不正确,其理由是若有四氧化三铁(Fe3O4)存在,现象相同(或者不能证明没有四氧化三铁(Fe3O4),合理即可).
查阅资料知道:
Fe3O4溶于稀盐酸生成FeCl3、FeCl2和水,其反应方程式可表示为Fe3O4+8HCl=2FeCl3+FeCl2+4H2O
Fe3O4也能溶于稀硝酸(HNO3),反应生成Fe(NO3)3、NO和水,试写出反应的化学方程式3Fe3O4+28HNO3=9Fe(NO3)3+NO+14H2O.

(1)写出装置A玻璃管中发生反应的化学方程式:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO;
(2)整套装置还有一个明显的不足之处是:缺少尾气处理装置.
(3)B中得到的黑色产物W,该活动小组同学根据图2对产物W的成分进行探究.
【提出问题】黑色粉末W可能是什么呢?
【查阅资料】
①铁的氧化物有氧化铁,氧化亚铁和四氧化三铁等,其中氧化铁为红棕色,其余都为黑色.
②铁的氧化物中四氧化三铁有磁性,能被磁铁吸引.
③铁的氧化物都难溶于水,却都能与稀盐酸反应而被溶解.
④铁的氧化物通常情况下不与CuSO4溶液反应.
【进行猜想】
①甲同学认为黑色粉末W全部是铁粉.请写出生成铁的化学反应方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.该反应利用了CO的还原性.
②乙同学认为甲同学的猜想是错误的,理由是黑色粉末W与足量的硫酸铜溶液反应后仍有黑色固体存在.
③丙同学认为黑色粉末W中不含Fe2O3,理由是氧化铁是红棕色的固体.
丙同学提出如下猜想,请你结合所学知识帮他补充完整.
猜想1:黑色粉末W由铁粉和四氧化三铁(Fe2O3)组成;
猜想2:黑色粉末W由铁粉和氧化亚铁(FeO)组成;
猜想3:黑色粉末W由铁粉、四氧化三铁(Fe2O3)、氧化亚铁(FeO).
【实验探究】
| 方案 | 实验操作 | 可能的现象 | 结论 |
| ① | 取适量黑色粉末W用磁铁吸引 | 黑色粉末全部被吸引 | 猜想1正确 |
| ② | 取适量黑色粉末W用磁铁吸引 | 黑色粉末部分被吸引 | 猜想2正确 |
| ③ | 取适量黑色粉末R用加入足量稀盐酸 | 黑色粉末全部溶解 | 猜想3正确 |
| ④ | 取适量黑色粉末R用磁铁吸引 | 黑色固体部分被吸引 | 猜想4正确 |
【反思提高】
丁同学认为方案②和方案③中得出的结论不正确,其理由是若有四氧化三铁(Fe3O4)存在,现象相同(或者不能证明没有四氧化三铁(Fe3O4),合理即可).
查阅资料知道:
Fe3O4溶于稀盐酸生成FeCl3、FeCl2和水,其反应方程式可表示为Fe3O4+8HCl=2FeCl3+FeCl2+4H2O
Fe3O4也能溶于稀硝酸(HNO3),反应生成Fe(NO3)3、NO和水,试写出反应的化学方程式3Fe3O4+28HNO3=9Fe(NO3)3+NO+14H2O.
9.化学课堂上要学习碱的化学性质,老师让两位同学和他共同做实验,要求两位同学分别向澄清石灰水和氢氧化钠溶液中吹气,如图①②所示,老师告诉同学们,呼出的气体中只有二氧化碳有可能与澄清石灰水和氢氧化钠溶液反应
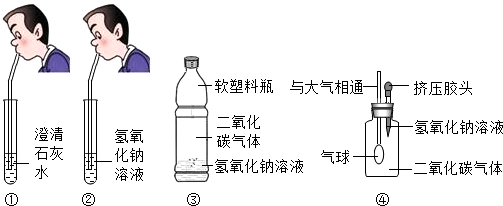
同学们在吹气后观察到①中澄清石灰水变浑浊,②中氢氧化钠溶液无明显现象,观察实验现象后老师问,通过实验现象的观察,检验二氧化碳气体应该使用澄清石灰水,针对②中的情況,师生共同开始探究之旅.
【提出问题】二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
【猜想假设】猜想A:西者发生了化学反应;猜想B:西者没有发生化学反应.
【实验探究】
(1)小明设计了如图所示的③、④两个实验.
实验现象:③中的软塑料瓶变瘪,④中气球变大.
(2)小亮认为小明的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低,小光同学却对此提出了质疑,他认为小明的实验不严谨,若仍利用该装置,需要补做的对比实验是将氢氧化钠溶液换成等体积的水,与加入氢氧化钠溶液的实验现象进行对比.
(3)小光设计实验验证实验②中溶质的成分,请帮他填写实验报告:
写出步骤 a发生反应的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl(或Na2CO3+BaCl2=BaCO3↓+2NaCl).
【反 思】氢氧化钠溶液必须密封保存.
氢氧化钠溶液暴露在空气中易变质的原因 (用化学方程表示)2NaOH+CO2=Na2CO3+H2O.

同学们在吹气后观察到①中澄清石灰水变浑浊,②中氢氧化钠溶液无明显现象,观察实验现象后老师问,通过实验现象的观察,检验二氧化碳气体应该使用澄清石灰水,针对②中的情況,师生共同开始探究之旅.
【提出问题】二氧化碳通入氢氧化钠溶液中无明显现象,两者是否发生了化学反应?
【猜想假设】猜想A:西者发生了化学反应;猜想B:西者没有发生化学反应.
【实验探究】
(1)小明设计了如图所示的③、④两个实验.
实验现象:③中的软塑料瓶变瘪,④中气球变大.
(2)小亮认为小明的实验是可行的,其共同原理是二氧化碳和氢氧化钠溶液反应,使容器内压强降低,小光同学却对此提出了质疑,他认为小明的实验不严谨,若仍利用该装置,需要补做的对比实验是将氢氧化钠溶液换成等体积的水,与加入氢氧化钠溶液的实验现象进行对比.
(3)小光设计实验验证实验②中溶质的成分,请帮他填写实验报告:
| 实验步骤 | 实验现象 | 结论 |
| a.取少许该溶液于试管中,滴入足量的CaCl2(或BaCl2)溶液 | 出现白色沉淀 | 溶质为碳酸钠和氢氧化钠 |
| b.静置上述溶液,取上层清液少许于另一只试管中,滴入几滴酚酞溶液 | 溶液变红 |
【反 思】氢氧化钠溶液必须密封保存.
氢氧化钠溶液暴露在空气中易变质的原因 (用化学方程表示)2NaOH+CO2=Na2CO3+H2O.
19.氯化钴是一种粉红色至红色结晶,它的无水物为蓝色.氯化钴在生活中的应用十分广泛,例如它可以在国防工业中用于制造毒气罩,在涂料工业中用于制造油漆催干剂等.已知氯化钴中,钴为+2价、氯为-1价,则它的化学式为( )
| A. | CoCl | B. | CoCl2 | C. | CoCl3 | D. | CoCl4 |
6.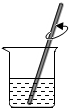 如图所示的是配制溶液过程中的某一项实验操作.下列是四位同学关于这项实验操作的说法,你认为其中不正确的是( )
如图所示的是配制溶液过程中的某一项实验操作.下列是四位同学关于这项实验操作的说法,你认为其中不正确的是( )
 如图所示的是配制溶液过程中的某一项实验操作.下列是四位同学关于这项实验操作的说法,你认为其中不正确的是( )
如图所示的是配制溶液过程中的某一项实验操作.下列是四位同学关于这项实验操作的说法,你认为其中不正确的是( )| A. | 这个实验操作的名称为搅拌溶解 | |
| B. | 再溶解溶质时,该操作可以加快实验进程 | |
| C. | 玻璃棒可以使难溶解的溶质变为易溶解的溶质 | |
| D. | 在配置氯化钠溶液时,玻璃棒不会影响水所能溶解的氯化钠的量 |
3.下列鉴别物质的试剂或方法,不正确的是( )
| 序号 | 待鉴别的物质 | 鉴别试剂或方法 |
| A | 氧化铜与氧化铁 | 观察颜色 |
| B | 硝酸铵与食盐固体 | 水 |
| C | 氢氧化钠溶液与碳酸钠溶液 | 酚酞溶液 |
| D | 氧气与二氧化碳 | 带火星的木条 |
| A. | A | B. | B | C. | C | D. | D |