题目内容
6.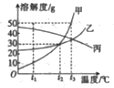 如图是甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法正确的是B
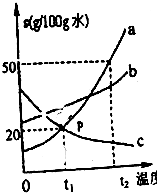
如图是甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法正确的是BA、t2℃时,将20g乙物质加入50g水中,充分溶解后的溶液为不饱和溶液
B、t3℃时,将甲、乙的饱和溶液降温至t2℃,所得溶液中溶质的质量分数相等
C、t3℃时,将甲、丙的饱和溶液恒温蒸发10g水后,前者析出晶体而后者无晶体析出
D、t3℃时,10g甲物质中加20g水,充分溶解后再降温到t2℃,所得溶液的质量是26g.
分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而丙的溶解度随温度的升高而减少;t2℃时,乙的溶解度是30g,因此将20g乙物质加入50g水中,充分溶解后的溶液为饱和溶液,不饱和溶液错误;t3℃时,将甲、乙的饱和溶液降温至t2℃,所得溶液中溶质的质量分数相等正确,因为降温后甲和乙的溶解度相等;t3℃时,将甲、丙的饱和溶液恒温蒸发10g水后,前者析出晶体而后者无晶体析出错误,都有晶体析出;t3℃时,甲的溶解度是50g,10g甲物质中加20g水,充分溶解后再降温到t2℃析出4g固体,所得溶液的质量=30g-4g=26g.
解答 解:A、t2℃时,乙的溶解度是30g,因此将20g乙物质加入50g水中,充分溶解后的溶液为饱和溶液,不饱和溶液错误;故选项错误;
B、t3℃时,将甲、乙的饱和溶液降温至t2℃,所得溶液中溶质的质量分数相等正确,因为降温后甲和乙的溶解度相等;故选项正确;
C、t3℃时,将甲、丙的饱和溶液恒温蒸发10g水后,前者析出晶体而后者无晶体析出错误,都有晶体析出;故选项错误;
D、t3℃时,甲的溶解度是50g,10g甲物质中加20g水,充分溶解后再降温到t2℃析出4g固体,所得溶液的质量=30g-4g=26g;故答案为:26;
故选B;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
14.下列反应中有一种物质既是氧化剂又是还原剂的是( )
| A. | 2KI+Br2=2KBr+I2 | B. | 2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑ | ||
| C. | Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O | D. | 2Na2O2+2H2O=4NaOH+O2↑ |
11.如图所示的实验操作能达到实验目的是( )
| A. | 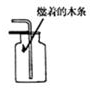 用燃着的木条检验二氧化碳 | B. |  加热蒸发食盐水 | ||
| C. | 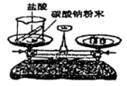 用盐酸和碳酸钠反应验证质量守恒 | D. | 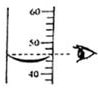 用量筒试量取46mL的水 |
 人类的生存、发展离不开化学.请你回答下列问题.
人类的生存、发展离不开化学.请你回答下列问题.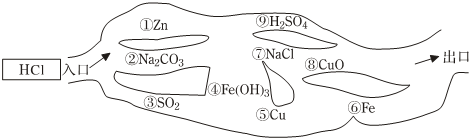
 归纳是学习科学的重要方法,总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白:
归纳是学习科学的重要方法,总结出如图所示的物质之间的反应关系(图中短线连接的物质表示能相互反应),请帮助完成下列空白: