题目内容
16.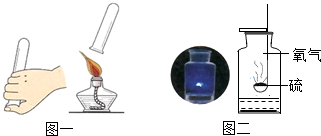 (1)如图一所示的试管中盛装的是氢气,则该实验的目的是检验氢气的纯度.
(1)如图一所示的试管中盛装的是氢气,则该实验的目的是检验氢气的纯度.(2)如图二所示是硫在氧气中燃烧实验,实验中会观察到硫燃烧产生(明亮的)蓝紫色色火焰;瓶中所装水的作用是吸收有毒的二氧化硫气体,如果能将水换成一种溶液则效果更好,该反应的化学方程式为SO2+2NaOH═Na2SO3+H2O.
分析 (1)根据所进行的操作来判断实验目的;
(3)根据硫燃烧时所产生的现象来分析原因,并考虑二氧化硫的性质来选择吸收方法
解答 解:(1)该实验的目的是检验氢气的纯度,以防点燃时发生爆炸;
(2)硫燃烧产生明亮的蓝紫色火焰,同时要放出热量,二氧化硫可以和碱的溶液发生反应,所以可以选择氢氧化钠溶液来吸收二氧化硫,会取得更好的效果.
故答案为:(1)检验氢气的纯度;(2)(明亮的)蓝紫色;SO2+2NaOH═Na2SO3+H2O
点评 熟练掌握常见实验操作和有关的实验现象以及注意事项是解决此题的关键.

练习册系列答案
相关题目
4.下列用品使用的材料不属于合成材料的是( )
| A. | 塑料袋 | B. | 汽车轮胎 | C. | 尼龙绳 | D. | 不锈钢餐具 |
1.如图所示实验操作正确的是( )
| A. |  滴加少量液体 | B. |  闻气体气味 | C. | 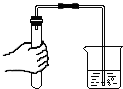 检查气密性 | D. | 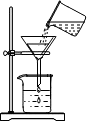 过滤 |
8.在一次化学实验中,同学们将饱和硫酸铜溶液逐滴加到5mL饱和NaOH溶液中,观察到如表异常实验现象:
已知蓝色沉淀是氢氧化铜,写出生成蓝色沉淀的化学方程式CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
【提出问题】
实验Ⅰ中蓝色沉淀为什么消失?
【查阅资料】
①氢氧化铜在室温下稳定,70℃~80℃时分解(产物有氧化铜).
②铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与假设】
针对实验Ⅰ中蓝色沉淀为什么消失,同学们提出如下两个猜想:
猜想①:蓝色沉淀消失可能是氢氧化铜发生分解反应.
猜想②:蓝色沉淀消失可能是氢氧化铜溶解在NaOH溶液中,形成亮蓝色溶液.
甲同学认为猜想①不成立,理由是氢氧化铜分解生成黑色的氧化铜固体.
【实验验证】
乙同学为验证猜想②,进行了如表实验.
【解释与结论】
(1)1号试管中现象为蓝色固体不消失.
(2)上述实验得出的结论是氢氧化铜能溶解在高于20%的NaOH中形成亮蓝色溶液.
(3)进一步查阅资料可知,氢氧化铜在NaOH溶液中溶解生成铜酸钠,反应的化学方程式为2NaOH+Cu(OH)2=Na2Cu(OH)4.
【反思与评价】
针对实验Ⅱ,丙同学推测,饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是蓝色沉淀逐渐变为黑色.
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| Ⅰ | 第1~6滴 | 有蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| Ⅱ | 第7~9滴 | 产生蓝色沉淀,且沉淀逐渐增多,振荡后沉淀不消失,但沉淀很快变成黑色 |
【提出问题】
实验Ⅰ中蓝色沉淀为什么消失?
【查阅资料】
①氢氧化铜在室温下稳定,70℃~80℃时分解(产物有氧化铜).
②铜酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与假设】
针对实验Ⅰ中蓝色沉淀为什么消失,同学们提出如下两个猜想:
猜想①:蓝色沉淀消失可能是氢氧化铜发生分解反应.
猜想②:蓝色沉淀消失可能是氢氧化铜溶解在NaOH溶液中,形成亮蓝色溶液.
甲同学认为猜想①不成立,理由是氢氧化铜分解生成黑色的氧化铜固体.
【实验验证】
乙同学为验证猜想②,进行了如表实验.
| 实验操作 | 实验现象 |
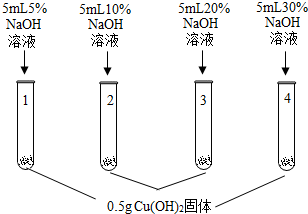 | 1号试管,… 2号试管,蓝色固体不消失 3号试管,蓝色固体减少 4号试管,蓝色固体消失,得到亮蓝色溶液 |
(1)1号试管中现象为蓝色固体不消失.
(2)上述实验得出的结论是氢氧化铜能溶解在高于20%的NaOH中形成亮蓝色溶液.
(3)进一步查阅资料可知,氢氧化铜在NaOH溶液中溶解生成铜酸钠,反应的化学方程式为2NaOH+Cu(OH)2=Na2Cu(OH)4.
【反思与评价】
针对实验Ⅱ,丙同学推测,饱和硫酸铜溶液与饱和氢氧化钠溶液的反应是放热反应,他依据的实验现象是蓝色沉淀逐渐变为黑色.
6.分类法是化学学习的重要方法.下列说法正确的是( )
| A. | 烧碱、纯碱、热石灰是常见的碱 | |
| B. | 蛋白质、合成纤维、油脂是常见的营养物质 | |
| C. | 生石灰、碱石灰、浓硫酸都可用作干燥剂 | |
| D. | 尿素、硝酸钾、磷酸二氢铵都可作复合肥料 |
 近日,网络上出现了“不锈钢水壶中的锰会让人智力低下”等传言.对此,国家食品安全专家钟凯作了解答.“不锈钢材质中的锰含量与迁移量没有任何必然联系,合金状态下,金属的惰性会增强.”钟凯指出,食品接触材料的重金属迁移量是用强酸、强碱、有机溶剂等,在较高温度下长时间浸泡模拟出来的,如果这种状态下迁移量都没问题,日常使用根本不是问题.
近日,网络上出现了“不锈钢水壶中的锰会让人智力低下”等传言.对此,国家食品安全专家钟凯作了解答.“不锈钢材质中的锰含量与迁移量没有任何必然联系,合金状态下,金属的惰性会增强.”钟凯指出,食品接触材料的重金属迁移量是用强酸、强碱、有机溶剂等,在较高温度下长时间浸泡模拟出来的,如果这种状态下迁移量都没问题,日常使用根本不是问题.