题目内容
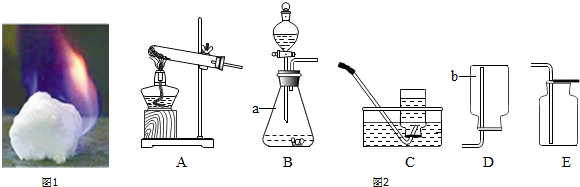
14.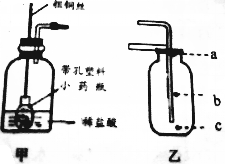 文文同学收集了一些家庭装修时废弃的大理石碎片,并查阅资料得知铜与稀硫酸、盐酸不反应,铁丝可以与稀硫酸和盐酸反应.于是他设计了如图的甲、乙两装置来制取二氧化碳,请回答下列问题:
文文同学收集了一些家庭装修时废弃的大理石碎片,并查阅资料得知铜与稀硫酸、盐酸不反应,铁丝可以与稀硫酸和盐酸反应.于是他设计了如图的甲、乙两装置来制取二氧化碳,请回答下列问题:(1)大理石应放在带孔塑料小药瓶中;
(2)装置中的粗铜丝不能(“能”或“不能”)用粗铁丝代替;
(3)文文骄傲的告诉同伴,他设计的装置可以随时控制反应的发生与停止,请你叙述其工作原理:通过上下移动粗铜丝,可以随时控制反应的发生与停止.
(4)用装置乙收集二氧化碳,验满时应把燃着的木条放在(选填字母)a处.
分析 制取装置包括加热和不需加热两种,实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.大理石应放在带孔塑料小药瓶中,装置中的粗铜丝不能用粗铁丝代替,因为铁丝与盐酸反应;甲装置的工作原理是:通过上下移动粗铜丝,可以随时控制反应的发生与停止;用装置乙收集二氧化碳,验满时应把燃着的木条放在a处,即放在集气瓶口.
解答 解:(1)大理石应放在带孔塑料小药瓶中,故答案为:带孔塑料小药瓶;
(2)装置中的粗铜丝不能用粗铁丝代替,因为铁丝与盐酸反应;故答案为:不能;
(3)甲装置的工作原理是:通过上下移动粗铜丝,可以随时控制反应的发生与停止;故答案为:通过上下移动粗铜丝,可以随时控制反应的发生与停止;
(4)用装置乙收集二氧化碳,验满时应把燃着的木条放在a处,即放在集气瓶口;故答案为:a;
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
6.2014年4月,兰州市局部自来水中苯(C6H6)含量严重超标,引发市民恐慌,苯的沸点为80.1℃,熔点为5.5℃,难溶于水,有剧毒,下列有关苯的说法中正确的是( )
| A. | 苯不属于有机物 | |
| B. | 苯是由6个碳原子和6个氢原子构成的 | |
| C. | 可通过加热蒸发的方法除去水中的苯 | |
| D. | 常温下可通过滤纸过滤的方法除去水中的苯 |
3.下列说法中不正确的是( )
| A. | 河水经过沉淀、过虑、活性炭吸附等净化处理后,得到的水是纯水 | |
| B. | 硬水和软水可用肥皂水区分 | |
| C. | 洗涤剂能洗涤餐具上油污的原因是洗涤剂可以使油脂乳化 | |
| D. | 实验室中含有盐酸的废水不可以直接倒入铸铁下水管道 |
4.小明和他的同学在实验室发现上一次实验后忘记塞上瓶塞的氢氧化钠溶液的试剂瓶瓶口周围有一些白色固体.他们怀疑氢氧化钠溶液已经变质,于是进行了如下实验探究.
【提出问题】氢氧化钠溶液是否变质?
【提出猜想】
①该氢氧化钠溶液没有变质;②该氢氧化钠溶液部分变质;③该氢氧化钠溶液全部变质.
【实验验证】
【讨论】小明同学认为,根据上述实验(1)(2)可推断,猜想②正确.而小张则认为猜想③也可能正确,理由是碳酸钠溶液也能使酚酞溶液变红.于是小王又设计了如下补充实验:
(1)取原溶液少量于试管中,逐滴加入BaCl2溶液至不再产生沉淀.静置,分层.
(2)取上层清液,向其中加入CuSO4溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式:CuSO4+2NaOH═Na2SO4+Cu(OH)2↓.反之则说明氢氧化钠溶液已经全部变质.
【提出问题】氢氧化钠溶液是否变质?
【提出猜想】
①该氢氧化钠溶液没有变质;②该氢氧化钠溶液部分变质;③该氢氧化钠溶液全部变质.
【实验验证】
| 操作 | 现象 | 结论 | 化学方程式 | |
| (1) | 取少量溶液于试管中,滴加无色酚酞溶液 | 无色酚酞变红 | 溶液显碱性 | / |
| (2) | 取少量溶液于试管中,滴加稀盐酸 | 有气泡产生 | 溶液中存在碳酸钠 | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
(1)取原溶液少量于试管中,逐滴加入BaCl2溶液至不再产生沉淀.静置,分层.
(2)取上层清液,向其中加入CuSO4溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式:CuSO4+2NaOH═Na2SO4+Cu(OH)2↓.反之则说明氢氧化钠溶液已经全部变质.
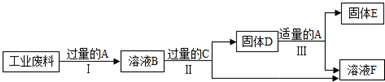
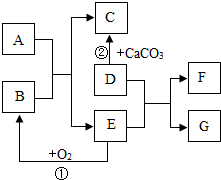 已知A-G为中学化学中常见物质,它们之间有如图所示的转化关系(部分生成物已略去),其中A、E、F为单质,A、E为固体,E为产量最大的金属,C、F为气体,反应②为实验室制取C的方法.请回答下列问题:
已知A-G为中学化学中常见物质,它们之间有如图所示的转化关系(部分生成物已略去),其中A、E、F为单质,A、E为固体,E为产量最大的金属,C、F为气体,反应②为实验室制取C的方法.请回答下列问题: