题目内容
14. 石灰石是常用的建筑材料.
石灰石是常用的建筑材料.甲乙同学设计了如下实验方案进行探究:
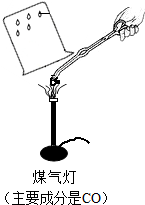
Ⅰ.甲同学取石灰石按图所示进行实验(煤气灯能达到石灰石分解的温度),
观察到烧杯内壁石灰水变浑浊,由此甲同学认为石灰石已分解.
甲同学结论不合理的理由是煤气灯的燃料的主要成分为一氧化碳,而一氧化碳燃烧生成了二氧化碳,所以澄清石灰水变浑浊不一定是来源于石灰石的分解.
写出石灰水变浑浊的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O.
Ⅱ.乙同学进行如下实验,完成下表:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量煅烧后固体于试管中,加水振荡,过滤,取滤液,滴加酚酞溶液 | 溶液变红 | 证明固体中含有氧化钙 |
| 取滤渣滴加足量的稀盐酸 | 有气泡产生 | 含有碳酸钙 |
①根据方案计算石灰石中碳酸钙的质量分数(根据化学方程式列式计算).
②指出该实验方案中一处明显的不足并说明原因氧化钙会吸收空气中的水分.
分析 Ⅰ、根据一氧化碳燃烧也会生成二氧化碳,对二氧化碳的检验也会造成干扰进行分析;
根据氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水进行分析;
Ⅱ、根据氧化钙和水会生成氢氧化钙,氢氧化钙能使酚酞变红色,盐酸和碳酸钙反应会生成二氧化碳气体进行分析;
Ⅲ、根据质量守恒定律计算生成二氧化碳的质量,依据化学方程式进行计算,以及氧化钙有吸水性进行分析.
解答 解:Ⅰ、一氧化碳燃烧也会生成二氧化碳,对二氧化碳的检验也会造成干扰,所以甲同学结论不合理的理由是:一氧化碳燃烧也能产生二氧化碳,使石灰水变浑浊的二氧化碳不一定来自于石灰石分解;
氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
Ⅱ、氧化钙和水会生成氢氧化钙,氢氧化钙能使酚酞变红色,盐酸和碳酸钙反应会生成二氧化碳气体,所以
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量煅烧后固体于试管中,加水振荡,过滤,取滤液,滴加酚酞溶液 | 溶液变红 | 证明固体中 含有氧化钙 |
| 取滤渣滴加足量的稀盐酸 | 有气泡产生 | 含有碳酸钙 |
Ⅱ设参加反应的碳酸钙质量为x
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
x 3.96g
$\frac{100}{x}$=$\frac{44}{3.96}$
x=9g
所以石灰石中碳酸钙的质量分数为:$\frac{9g}{10g}$×100%=90%
氧化钙有吸水性,不能在空气中冷却至室温,否则会增大剩余固体的质量,使碳酸钙的质量分数产生误差.
故答案为:Ⅰ、一氧化碳燃烧也能产生二氧化碳,使石灰水变浑浊的二氧化碳不一定来自于石灰石分解;
CO2+Ca(OH)2→CaCO3↓+H2O;
Ⅱ、氧化钙和水会生成氢氧化钙,氢氧化钙能使酚酞变红色,盐酸和碳酸钙反应会生成二氧化碳气体,所以
| 实验步骤 | 实验现象 | 实验结论 |
| 酚酞 | 氧化钙 | |
| 有气泡产生 |
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中所给的提示进行解答.

练习册系列答案
 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目
8.为中国科学家屠呦呦点赞!她因创制新型抗疟药青蒿素而获得诺贝尔医学奖.下列关于青蒿素(C15H22O5)的说法不正确的是( )
| A. | 每个靑蒿素分子中含有42个原子 | B. | 靑蒿素由三种元素组成 | ||
| C. | 靑蒿素属于有机化合物 | D. | 青蒿索中C、H元素的质量比为15:22 |
5.某同学在做“铁丝在氧气中燃烧”实验时未燃烧起来,其原因是( )
| A. | 铁丝绕成螺旋状 | B. | 铁丝一端系上火柴梗 | ||
| C. | 铁丝表面附有油漆 | D. | 火柴梗临近烧完时才放入集气瓶 |
9.欲除去不纯物质中的杂质(括号内为杂质),所用试剂和方法均正确的是
( )
| 选项 | 待提纯物质 | 选用试剂 | 操作方法 |
| A | NH3(H2O) | 浓硫酸 | 洗气 |
| B | NaCl(KNO3) | 水 | 溶解、降温结晶、过滤 |
| C | CaCl2溶液(HCl) | CaCO3 | 过滤 |
| D | Cu(Fe) | 稀硫酸 | 过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
6.可以把NaOH、H2SO4和Ca(OH)2一次鉴别出来的试剂是( )
| A. | 酚酞试液 | B. | BaCl2溶液 | C. | Na2CO3溶液 | D. | AgNO3溶液 |
3.下列各组溶液,不用其他试剂就不能鉴别出来的是( )
| A. | FeCl3、KOH、MgSO4、KCl | B. | NaCl、AgNO3、稀HCl、稀HNO3 | ||
| C. | NaOH、稀HCl、CuSO4、NaNO3 | D. | Na2CO3、稀HCl、BaCl2、Na2SO4 |
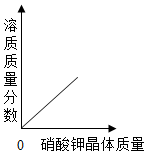
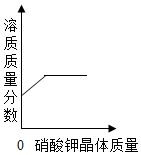
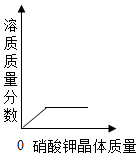
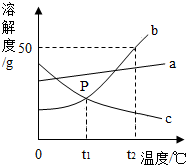 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题: