题目内容
12.学习化学后,我们学会了从微观角度认识物质.(1)氧原子的结构示意图为:

(2)Na+和钠原子中相等的是AD(填序号).
A.质子数 B.电子数 C.最外层电子数 D.中子数
(3)保持一氧化碳化学性质的粒子名称是一氧化碳分子.
分析 (1)根据氧原子的核外电子的排布特点作出氧原子的结构示意图;
(2)根据Na+和钠原子结构特点分析;
(3)根据分子的定义和一氧化碳的构成分析.
解答 解:(1)氧原子的核内质子数是8,核外有两个电子层,第一层有2个电子,第二层有6个电子,原子的结构示意图为: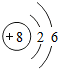 ;
;
(2)钠原子失去一个电子转化为Na+,Na+和钠原子中相等的是质子数和中子数;
(3)保持一氧化碳化学性质的粒子名称是一氧化碳分子.
故答为:(1)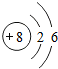 ;(2)AD;(3)一氧化碳分子.
;(2)AD;(3)一氧化碳分子.
点评 能够从宏观和微观两个方面正确地认识物质.从宏观上,物质都是由元素组成的;从微观上,物质是由原子或分子或离子构成的.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.不能用来区分二氧化碳和一氧化碳的方法是( )
| A. | 澄清石灰水 | B. | 燃着的木条 | C. | 稀盐酸 | D. | 紫色石蕊试液 |
3.为探究气体X的组成,某兴趣小组进行如图所示实验(固定装置未画出).
【资料在线】
①加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
②碱石灰为固体氢氧化钠和氢氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X.
③本实验条件下,氮气密度为1.15g•L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.
【实验步骤】
①连接仪器,并检查装置气密性.
②取一定量氧化铜,准确称得其质量为2.40g.
③按图所示装入药品(其中B、C管中分别装入的是足量碱石灰和足量无水氯化钙),测得相关的量记录在数据Ⅰ(见表).
④连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却后,再次测量并记录相关数据Ⅱ(见表).
【实验装置】

【相关数据】
回答问题:
(1)B中装置中氧化钙吸水的原理为CaO+H2O═Ca(OH)2(用化学方程式表示);
(2)实验过程中,当观察到黑色固体全部变红,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是防止生成的铜被氧化;
(3)分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.由此推知,气体X中一定没有(填“有”或“没有”)氧元素.
④读取量气管中氮气体积之前需要调节量气管和水准管液面相平,通过计算推导出气体X的化学式为NH3.
【资料在线】
①加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
②碱石灰为固体氢氧化钠和氢氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X.
③本实验条件下,氮气密度为1.15g•L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.
【实验步骤】
①连接仪器,并检查装置气密性.
②取一定量氧化铜,准确称得其质量为2.40g.
③按图所示装入药品(其中B、C管中分别装入的是足量碱石灰和足量无水氯化钙),测得相关的量记录在数据Ⅰ(见表).
④连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却后,再次测量并记录相关数据Ⅱ(见表).
【实验装置】

【相关数据】
| 测量项目/数据编号 | Ⅰ | Ⅱ |
| 玻璃管(含药品)的质量/g | 52.40 | 51.92 |
| B装置(含药品)的质量/g | 102.00 | 102.54 |
| 氮气的体积/mL | / | 243.5 |
(1)B中装置中氧化钙吸水的原理为CaO+H2O═Ca(OH)2(用化学方程式表示);
(2)实验过程中,当观察到黑色固体全部变红,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是防止生成的铜被氧化;
(3)分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.由此推知,气体X中一定没有(填“有”或“没有”)氧元素.
④读取量气管中氮气体积之前需要调节量气管和水准管液面相平,通过计算推导出气体X的化学式为NH3.
17.下列事实与相应的解释不一致的是( )
| 选项 | 事实 | 解释 |
| A | 50mL水和50mL酒精混合后的体积小于100mL | 分子间有间隔 |
| B | 氧气和臭氧(O3)性质不完全相同 | 构成物质的分子不同 |
| C | 稀有气体的化学性质稳定 | 原子的最外层电子达到相对稳定结构 |
| D | 铁丝在空气中不燃烧,在氧气中却可以燃烧 | 物质的种类决定反应的剧烈程度 |
| A. | A | B. | B | C. | C | D. | D |
2.下列对质量守恒定律的理解或运用,观点合理的是( )
| A. | 10g冰受热融化成10g水,体现了这一变化遵循质量守恒定律 | |
| B. | “2L氢气和1L氧气在一定条件下反应,一定会生成3L水”是由质量守恒定律决定的 | |
| C. | 3g碳放入装有10g氧气的密闭容器中,充分反应后一定生成13g二氧化碳 | |
| D. | “蜡炬成灰泪始干”的描述涉及化学变化中物质质量变化的现象不违背质量守恒定律 |

 甲、乙两种固体的溶解度曲线如图,请回答下列问题:
甲、乙两种固体的溶解度曲线如图,请回答下列问题: