题目内容
19.下列化肥中含氮元素质量分数最小的是( )| A. | NH4Cl | B. | CO(NH2)2 | C. | NH4HCO3 | D. | (NH4)2SO4 |
分析 根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,据此进行解答.
解答 解:A、NH4Cl中氮元素的质量分数为$\frac{14}{14+1×4+35.5}$×100%=$\frac{14}{53.5}×$100%.
B、CO(NH2)2中氮元素的质量分数为$\frac{14×2}{12+16+(14+1×2)×2}$×100%=$\frac{14×2}{60}$×100%=$\frac{14}{30}×$100%.
C、NH4HCO3中氮元素的质量分数为$\frac{14}{14+1×4+1+12+16×3}$×100%=$\frac{14}{79}$×100%.
D、(NH4)2SO4中氮元素的质量分数为$\frac{14×2}{(14+1×4)×2+32+16×4}$×100%=$\frac{14}{132}$×100%=$\frac{14}{66}$×100%.
故含氮元素质量分数最小的是C.
故选:C.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
14.某兴趣小组的同学对一包久置的生石灰(CaO)干燥剂产生了好奇,于是他们对这包干燥剂的成分展开了探究.
【提出问题】
这包干燥剂是否变质,成分是什么?
【猜想假设】
猜想一:全部是CaO;
猜想二:是CaO和Ca(OH)2的混合物;
猜想三:全部是Ca(OH)2;
猜想四:是Ca(OH)2和CaCO3的混合物.
【实验探究】
(1)取部分该干燥剂于试管中,加水后无放热现象,说明这包干燥剂中不含CaO.
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有CaCO3.
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下三种方案.
另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于3支试管中.请你参与实验,并填写表中的空白:
写出方案二发生的化学反应方程式:Ca(OH)2+CO2═CaCO3↓+H2O.
【实验结论】
通过以上实验探究,得出猜想四成立.
【拓展迁移】
小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注密封保存.
【提出问题】
这包干燥剂是否变质,成分是什么?
【猜想假设】
猜想一:全部是CaO;
猜想二:是CaO和Ca(OH)2的混合物;
猜想三:全部是Ca(OH)2;
猜想四:是Ca(OH)2和CaCO3的混合物.
【实验探究】
(1)取部分该干燥剂于试管中,加水后无放热现象,说明这包干燥剂中不含CaO.
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有CaCO3.
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下三种方案.
另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于3支试管中.请你参与实验,并填写表中的空白:
| 实验方案 | 方案一 | 方案二 | 方案三 |
| 实验操作 | 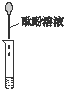 | 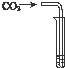 | 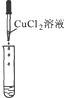 |
| 实验现象 | 溶液由无色变红色 | 澄清溶液变浑浊 | 产生蓝色絮状沉淀 |
【实验结论】
通过以上实验探究,得出猜想四成立.
【拓展迁移】
小组同学反思了生石灰干燥剂变质的原因,认识到实验室保存氧化钙应注密封保存.
11.将混有少量氧化铜粉末的铁粉放入盛有稀硫酸的烧杯中充分反应后,有部分铁粉剩余,过滤,则滤液中的溶质是( )
| A. | H2SO4 | B. | CuSO4和FeSO4 | C. | H2SO4和FeSO4 | D. | FeSO4 |
9. 如图所示,将一小块金属钠投入盛有蒸馏水的烧杯中,金属钠很快熔成一个白色小球,并浮在水面上急速游动,直至消失.化学方程式是:2Na+2H2O═2NaOH+H2↑.下列说法错误的是( )
如图所示,将一小块金属钠投入盛有蒸馏水的烧杯中,金属钠很快熔成一个白色小球,并浮在水面上急速游动,直至消失.化学方程式是:2Na+2H2O═2NaOH+H2↑.下列说法错误的是( )
 如图所示,将一小块金属钠投入盛有蒸馏水的烧杯中,金属钠很快熔成一个白色小球,并浮在水面上急速游动,直至消失.化学方程式是:2Na+2H2O═2NaOH+H2↑.下列说法错误的是( )
如图所示,将一小块金属钠投入盛有蒸馏水的烧杯中,金属钠很快熔成一个白色小球,并浮在水面上急速游动,直至消失.化学方程式是:2Na+2H2O═2NaOH+H2↑.下列说法错误的是( )| A. | 该反应属于置换反应 | |
| B. | 金属钠的密度比水小 | |
| C. | 反应后向烧杯中滴加硫酸铜溶液,会有红褐色沉淀生成 | |
| D. | 反应后向烧杯中滴加无色酚酞试液,溶液变红色 |