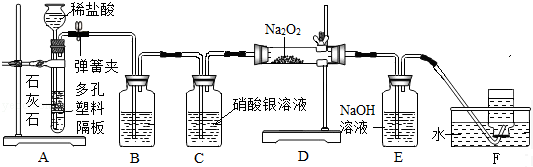
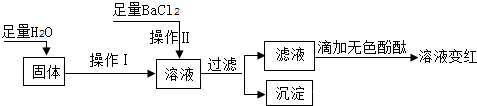
题目内容
1.氢能是一种极具发展潜力的清洁能源.以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法.其反应过程如图所示: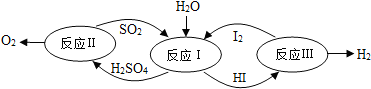
(1)反应I中,发生反应的化学方程式为SO2+2H2O+I2$\frac{\underline{\;太阳能\;}}{\;}$H2SO4+2HI.
(2)反应Ⅲ中,反应前后化合价发生改变的元素是H、I.
(3)在整个反应过程中,SO2、H2SO4、I2、HI都在循环使用,则制得H2中氢元素最初来源于H2O(填化学式).
分析 (1)根据反应I为二氧化硫与碘发生氧化还原反应生成硫酸和HI进行分析;
(2)根据单质中元素的化合价为零分析;
(3)根据质量守恒定律分析解答.
解答 解:(1)由图可知,反应I为二氧化硫与碘发生氧化还原反应生成硫酸和HI,该故答案为:SO2+2H2O+I2=H2SO4+2HI;
(2)反应Ⅲ中,H和I由化合态变为游离态,元素的化合价发生了改变;
(3)反应I的化学方程式为:SO2+2H2O+I2$\frac{\underline{\;太阳能\;}}{\;}$H2SO4+2HI,根据质量守恒定律可知,制得H2中氢元素最初来源于水;
故答案为:(1)SO2+2H2O+I2$\frac{\underline{\;太阳能\;}}{\;}$H2SO4+2HI;(2)H;I;(3)H2O.
点评 本题考查化学方程式的书写,元素的化合价等知识,难度不大.

练习册系列答案
相关题目
18.下列图示的实验操作,正确的是( )
| A. | 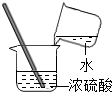 稀释浓硫酸 | B. | 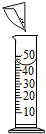 配制氯化钠溶液 | C. | 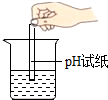 测定溶液pH | D. |  蒸发食盐水 |
9.燃着的火柴在空气中用力甩一下能熄灭,其原因是( )
| A. | 供给的氧气减少 | B. | 供给的氧气增加 | ||
| C. | 使温度降到火柴棍的着火点以下 | D. | 使火柴棍的着火点降低 |
13.水是我们身边重要的物质,下列说法不正确的是( )
| A. | 可用肥皂水区别硬水和软水 | |
| B. | H2O是由一个氢分子和一个氧原子构成 | |
| C. | H2O中氧元素的化合价为-2 | |
| D. | H2O是氧化物 |
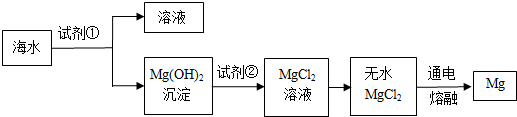
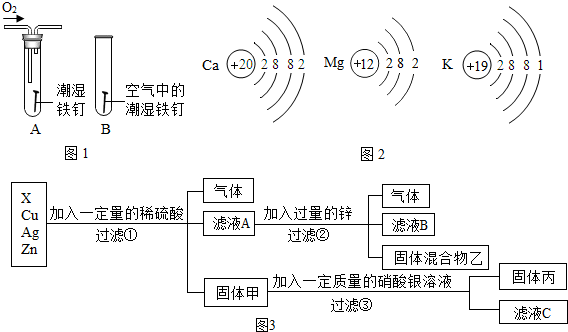
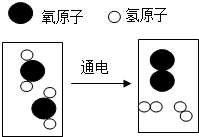 在物质的宏观性质、微观组成(或结构)和表示符号之间建立联系是化学学科的特点.某化学反应的微观示意图(表示氧原子,表示氢原子)如图:
在物质的宏观性质、微观组成(或结构)和表示符号之间建立联系是化学学科的特点.某化学反应的微观示意图(表示氧原子,表示氢原子)如图: