题目内容
向某无色溶液中加入氯化钡溶液,有白色沉淀产生,加入稀硝酸后白色沉淀不溶解,原溶液中( )
| A、一定含有SO42- |
| B、一定含有Ag+ |
| C、含有SO42-和Ag+ |
| D、可能有SO42-或Ag+ |
考点:常见离子的检验方法及现象
专题:物质的检验、鉴别与推断
分析:能与氯化钡反应,产生白色沉淀,再加入足量稀硝酸,沉淀不溶解,则该无色溶液中可能含有硫酸根或银离子.
解答:解:某无色溶液加入氯化钡溶液后有白色沉淀,再加稀硝酸沉淀不消失,若原溶液中有Cl-,则会生成AgCl沉淀,若原溶液中有SO32-离子,则生成BaSO3沉淀,加稀硝酸,BaSO3沉淀被氧化为BaSO4沉淀,若溶液中有SO42-,则生成BaSO4沉淀,硫酸钡和氯化银都不溶于硝酸,所以原溶液中可能含有SO42-或 SO32- 或Ag+;
故选D.
故选D.
点评:本题考查了硫酸根离子的检验,侧重于检验方法的评价,注意把握常见离子的性质以及检验方法,检验时要排除其它离子的干扰,题目难度不大.

练习册系列答案
相关题目
下列各组物质能在pH=12的溶液中能大量共存的是( )
| A、Na2CO3、NaOH、CaCl2 |
| B、CaCl2、NaCl、KNO3 |
| C、NaOH、Na2SO4、H2SO4 |
| D、NaNO3、FeCl3、CuSO4 |
下列关于水的说法错误的是( )
| A、水分子是由氢原子和氧原子构成的 |
| B、水是由氢元素和氧元素组成的 |
| C、1个水分子是由两个氢原子和一个氧原子构成的 |
| D、水分子是由两个氢元素和一个氧元素构成的 |
物质在空气中发生缓慢氧化、燃烧的共同点是( )
| A、都放出热量 | B、都生成气体 |
| C、都有响声 | D、都发光 |
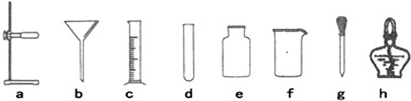
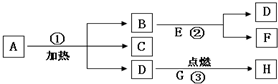 A、B…H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、G都是黑色固体,D能使带火星的木条复燃,E是一种无色液体,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变.试推断:
A、B…H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、G都是黑色固体,D能使带火星的木条复燃,E是一种无色液体,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变.试推断: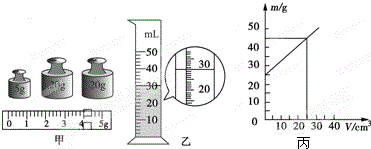 为确定某种未知液体的“身份”,科学教师把这个任务交给了小明的实验小组,他们利用天平和量筒进行了多次测量.某次的操作如下:
为确定某种未知液体的“身份”,科学教师把这个任务交给了小明的实验小组,他们利用天平和量筒进行了多次测量.某次的操作如下: 选用厨房中的下列物质填空(填序号):
选用厨房中的下列物质填空(填序号):