题目内容
11.张老师与同学们探究化学反应前后物质的质量关系,现请你一同参与:【提出问题】化学反应前后物质的质量总和是否相等?
【猜想假设】猜想1:各物质的质量总和不相等; 猜想2:各物质的质量总和相等.
【实验探究】同学们根据实验方案分组实验,用托盘天平分别称量反应前后物质的质量
| 实验方案一 | 实验方案二 |
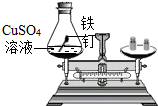 | 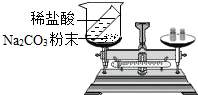 |
【分组实验二】稀盐酸与碳酸钠粉末反应的实验现象为有气泡产生,天平指针向右偏转.
【评价与反思】究竟哪种猜想正确?同学们分析两个方案的实验结果,通过讨论一致认为:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在密闭容器(或封闭体系等)中进行.
【得出结论】同学们进一步分析发现,反应体系中仪器和未参加反应的物质质量在反应前后保持不变,最终得出结论:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和.即猜想2正确.
分析 【分组实验一】根据金属活动性顺序,铁在铜的前面,能把铜置换出来解答;
【分组实验二】根据碳酸钠和稀盐酸反应有二氧化碳气体生成,由于气体逸出,反应前后称量质量不相等等知识进行分析;
【评价与反思】根据有气体参与和生成的反应,在验证质量守恒定律时应在密闭容器中进行解答;
【优化装置】根据装置特点进行分析解答;
【得出结论】根据质量守恒定律内容分析解答:参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和;
解答 解:
【分组实验一】将打磨干净的铁钉浸入CuSO4溶液中,铁与硫酸铜反应,生成硫酸亚铁和铜,实验现象为铁钉表面有红色物质析出,待溶液颜色发生改变时,再次称量,结果天平指针没有偏转;
【分组实验二】碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,根据质量守恒定律,参加反应的碳酸钠与氯化氢的质量和等于生成的氯化钠、水和二氧化碳的质量和,因有二氧化碳气体溢出,故反应后总质量比反应前总质量减少,观察到天平不平衡;
【评价与反思】通过讨论,同学们发现实验方案二中有气体溢出,导致指针向右偏转.得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡有气体生成或参加的反应一定要在密闭中进行.
【得出结论】参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和;
答案:
【分组实验一】铁钉表面有红色物质析出; 没有偏转;
【分组实验二】有气泡产生,天平指针向右偏转;
【评价与反思】密闭容器(或封闭体系等)
【结论与解释】参加化学反应.
点评 要验证质量守恒定律需根据反应物的状态和产物的状态选择敞口或密闭装置,若有气体参加或生成的反应需在密闭容器中进行.该题是对质量守恒定律的知识应用题,解题的关键是利用了反应前后元素的种类不会改变的知识.

练习册系列答案
相关题目
19.下列物质的用途与其化学性质相关的是( )
| A. | 碳用作冶炼金属 | B. | 石墨用于电极 | C. | 生铁铸造铁锅 | D. | 铜用于制造导线 |
1.对下列现象的解释或者结论错误的是( )
| A. | 湿衣服晾在太阳底下干得快--分子运动速率与温度有关 | |
| B. | 在钢铁制品表面涂油漆--可防止钢铁锈蚀 | |
| C. | 熄灭酒精灯应用灯帽盖灭--隔离可燃物 | |
| D. | 绿色植物的光合作用吸收CO2--是自然界碳循环中的重要一环 |




 打火机给人们的生活带来了方便,如图为普通打火机是示意图,请根据图示回答问题:
打火机给人们的生活带来了方便,如图为普通打火机是示意图,请根据图示回答问题: