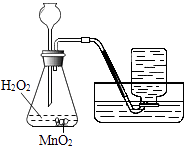
题目内容
【题目】根据下列如图1实验装置图,回答有关问题, 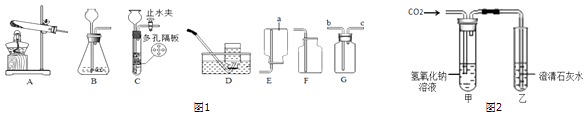
(1)装置图中仪器a的名称为 .
(2)用氯酸钾和二氧化锰混合共热制取较纯净的氧气,可选用的装置组合是 , 写出发生反应的化学方程式 . 若改用高锰酸钾制取氧气,发生装置应作的改动是 .
(3)实验室利用B装置制取二氧化碳的化学方程式为 , 如果利用G装置收集二氧化碳,气体应从端通入(填“b”或“c”),用C装置代替B装置,收集满气体后,C装置的操作是 .
(4)为研究二氧化碳会与氢氧化钠发生反应,采用图2装置进行实验,通入二氧化碳后,看到现象,说明二氧化碳与氢氧化钠发生反应;若对原装置改动继续实验,看到石灰水变浑浊,也能达到目的,改进的方法是; 若将二氧化碳通入氢氧化钠的酒精溶液,观察到溶液由澄清变浑浊,解释原因 .
【答案】
(1)集气瓶
(2)AD;2KClO3 ![]() 2KCl+3O2↑;在试管口加棉花
2KCl+3O2↑;在试管口加棉花
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;b;关闭止水夹
(4)石灰水不浑浊;将甲试管的进气改为短进长出(或将短导管延长至氢氧化钠溶液中);碳酸钠在酒精中的溶解度小,形成沉淀
【解析】解:(1)集气瓶是收集气体的仪器,所以答案是:集气瓶;(2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,用排水法收集的氧气比较纯净;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;所以答案是:AD;2KClO3 ![]() 2KCl+3O2↑;在试管口加棉花;(3)实验室制取CO2 , 是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;如果利用G装置收集二氧化碳,气体应从长管进入,因为二氧化碳的密度比空气大;用C装置代替B装置,收集满气体后,C装置的操作是:关闭止水夹;所以答案是:CaCO3+2HCl=CaCl2+H2O+CO2↑;b;关闭止水夹;(4)图2装置进行实验通入二氧化碳后,看到石灰水不浑浊,说明二氧化碳与氢氧化钠发生反应;改进的方法是:将甲试管的进气改为短进长出或将短导管延长至氢氧化钠溶液中;若将二氧化碳通入氢氧化钠的酒精溶液,观察到溶液由澄清变浑浊,解释原因:碳酸钠在酒精中的溶解度小,形成沉淀;所以答案是:石灰水不浑浊;将甲试管的进气改为短进长出(或将短导管延长至氢氧化钠溶液中);碳酸钠在酒精中的溶解度小,形成沉淀;
2KCl+3O2↑;在试管口加棉花;(3)实验室制取CO2 , 是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;如果利用G装置收集二氧化碳,气体应从长管进入,因为二氧化碳的密度比空气大;用C装置代替B装置,收集满气体后,C装置的操作是:关闭止水夹;所以答案是:CaCO3+2HCl=CaCl2+H2O+CO2↑;b;关闭止水夹;(4)图2装置进行实验通入二氧化碳后,看到石灰水不浑浊,说明二氧化碳与氢氧化钠发生反应;改进的方法是:将甲试管的进气改为短进长出或将短导管延长至氢氧化钠溶液中;若将二氧化碳通入氢氧化钠的酒精溶液,观察到溶液由澄清变浑浊,解释原因:碳酸钠在酒精中的溶解度小,形成沉淀;所以答案是:石灰水不浑浊;将甲试管的进气改为短进长出(或将短导管延长至氢氧化钠溶液中);碳酸钠在酒精中的溶解度小,形成沉淀;
【考点精析】认真审题,首先需要了解制取氧气的操作步骤和注意点(制取氧气的操作步骤(以高锰酸钾制取氧气并用排水法收集为例)a、步骤:查—装—定—点—收—移—熄),还要掌握二氧化碳的检验和验满(验证方法:将制得的气体通入澄清的石灰水,如能浑浊,则是二氧化碳.验满方法:用点燃的木条,放在集气瓶口,木条熄灭.证明已集满二氧化碳气体)的相关知识才是答题的关键.

 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案【题目】某实验小组利用如图实验装置探究二氧化碳的化学性质: 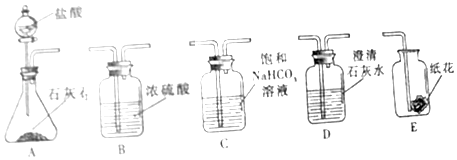
(1)请根据实验装置和实验内容,回答下面问题: ①探究二氧化碳与碱反应时,将装置A生成的二氧化碳气体通入装置D未出现浑浊,原因是;可将二氧化碳先通过装置 , 再通入装置D,理由是(用化学方程式表示);
②探究二氧化碳与水反应时,实验分两步进行:首先将二氧化碳通过石蕊溶液浸泡的干燥纸花,再将二氧化碳通过石蕊溶液浸泡的湿润纸花,这样做的目的是;结合上面实验,装置正确的连接顺序是(填序号)
(2)家庭生活中食品制作(如面条、馒头等)经常用到食用碱,食用碱的主要成分是碳酸钠,可能含有少量氯化钠.小莉将家中食用碱带到实验室进行探究,请设计实验验证小莉提供的食用碱样品是否含有氯化钠.
实验步骤 | 实验现象 | 结论与解释 |
1).取一定量的食用碱样品放入试管,加入蒸馏水、振荡 | 样品溶解 | 食用碱溶于水 |