题目内容
11.某露置于空气中的生石灰干燥剂,测得其中Ca元素质量分数为60%,向10g干燥剂中加足量稀盐酸使其完全溶解.正确的说法是( )| A. | 加入盐酸一定有气泡产生 | |
| B. | 生成CaCl2的物质的量为0.15mol | |
| C. | 此包干燥剂的组成可能是CaCO3 | |
| D. | 干燥剂的成分可能是Ca(OH)2、CaCO3的混合物 |
分析 生石灰能与水反应生成了氢氧化钙,氢氧化钙能与二氧化碳反应生成了碳酸钙,根据钙元素的质量分数判断混合物的组成,再根据物质的性质分析判断有关的说法.
解答 解:由于石灰能与水反应生成了氢氧化钙,氢氧化钙能与二氧化碳反应生成了碳酸钙.
氧化钙中钙元素的质量分数是:$\frac{40}{56}×100%$≈71%
氢氧化钙中钙元素的质量分数是:$\frac{40}{74}×100%$≈54%
碳酸钙中钙元素的质量分数是:$\frac{40}{100}×100%$=40%
由题意可知,测得其中Ca元素质量分数为60%,则该混合物可能是氧化钙与氢氧化钙的混合物,也有可能是氧化钙、氢氧化钙和碳酸钙的混合物.
A、若该混合物若是氧化钙与氢氧化钙的混合物,加入盐酸不产生气泡.故A错误;
B、钙元素的质量为:10g×60%=6g,钙元素物质的量是:$\frac{6g}{40g/mol}$=0.15mol,由质量守恒定律可知,生成CaCl2的物质的量为0.15mol.故B正确;
C、由上述分析,此包干燥剂的组成不可能是CaCO3,故C错误;
D、由上述分析可知,Ca(OH)2、CaCO3的混合物中钙的质量分数应在40%~54%之间,干燥剂的成分不可能是Ca(OH)2、CaCO3的混合物,故D错误.
故选B.
点评 本题主要考查了混合物成分的判断,熟悉氧化钙的性质及化学式的计算等知识是解答本题的关键.

练习册系列答案
相关题目
1.常用抗生素“先锋Ⅵ”为粉末状固体,每瓶含“先锋Ⅵ”0.5g,注射时应配成质量分数不高于20%的溶液,则使用时每瓶至少需加入蒸馏水( )
| A. | 4mL | B. | 3mL | C. | 2mL | D. | 1mL |
19.一定条件下,在一个密闭容器中发生某反应,测得反应过程中各物质的质量如下表所示,下列表述中错误的是( )
| 物质 | X | Y | Z | Q |
| 第一次测得的质量/g | 68 | 16 | 4.4 | 3.6 |
| 第二次测得的质量/g | 4 | 未测 | 48.4 | 39.6 |
| A. | 该反应一定是复分解反应 | B. | 若X为氧气,则Y一定发生氧化反应 | ||
| C. | 第二次测定时,Y已完全反应 | D. | 该反应中Z与Q质量变化之比为11:9 |
6.已知在一定条件下发生反应:甲十乙→丙+丁.下列判段正确的是( )
| A. | 若丙为Cu(NO3)2,则甲可能为Cu,也可能为CuO | |
| B. | 若丙为盐、丁为水.则该反应一定为复分解反应 | |
| C. | 若甲、丙为单质,乙、丁为化合物,则该反应可能为置换反应 | |
| D. | 甲、乙、丙、丁不可能含有同一种元素 |
16. a、b两种物质的溶解度曲线如图所示.下列说法正确的是( )
a、b两种物质的溶解度曲线如图所示.下列说法正确的是( )
 a、b两种物质的溶解度曲线如图所示.下列说法正确的是( )
a、b两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | 15℃时,a、b的溶液溶质质量分数相等 | |
| B. | 加水或升温均可使a、b的饱和溶液变为不饱和溶液 | |
| C. | 将15℃时b的饱和溶液升温至30℃,溶质质量分数不变 | |
| D. | 15℃时分别向100 g水中加入20 g a和b,降温至0℃,所得溶液均为饱和溶液 |
8.2015年10月,我国科学家屠呦呦由于发现了青蒿素(C15H22O5)而获得诺贝尔医学奖.下列有关青蒿素的说法不正确的是( )
| A. | 青蒿素是一种有机物 | B. | 青蒿素中碳、氢原子个数比为15:22 | ||
| C. | 青蒿素由三种元素组成 | D. | 青蒿素的相对分子质量为42 |
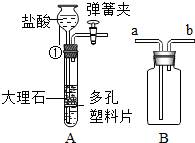 根据如图回答问题.
根据如图回答问题.