题目内容
17.写出下列反应的化学方程式:(1)水通电分解:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(2)红磷在氧气中燃烧:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)铁丝在氧气中燃烧:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(4)铜在氧气中受热:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;
以上反应属于化合反应的是(2)(3)(4)(填序号,下同),属于分解反应的是(1).
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.并根据反应特点确定反应的类型.
解答 解:(1)水通电生成氢气和氧气,是由一种物质生成两种物质,符合“一变多”的特征,属于分解反应;故填:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(2)红磷在氧气中燃烧的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,反应物是两种,生成物是一种,属于化合反应.故填:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(3)铁丝在氧气中燃烧的反应物是铁和氧气,生成物是四氧化三铁,反应条件是点燃,用最小公倍数法配平,所以方程式是:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,属于多变一的反应所以为化合反应;故答案为:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(4)铜在氧气中受热生成氧化铜,反应的方程式是:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,属于多变一的反应所以为化合反应.故填:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;
(2)(3)(4)符合多变一的特征,属于化合反应;(1)符合一变多的特征,属于分解反应.
故填:(2)(3)(4);(1).
点评 通过回答本题要知道书写化学方程式的步骤即注意事项,熟悉化合反应与分解反应的本质区别,并能灵活鉴别.

练习册系列答案
相关题目
7.蜡烛燃烧生成了二氧化碳和水,根据质量守恒定律得知蜡烛中一定含有的元素是( )
| A. | 碳 | B. | 氢 | C. | 碳、氢、 | D. | 碳、氢、氧 |
8.从宏观、微观和符号或图示三种水平上认识和理解化学知识,并建立三者之间的内在联系.请填写下表:
| 宏观现象 | 微观本质 | 符号或图示表达 |
| (1)温度升高压强不变,气体体积增大; | 温度升高,分子间的间隔变大 |  |
| (2)水通电分解,观察到电极表面都有气泡产生; | 水分子变成氢分子和氧分子 | 化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑. |
| (3)向氢氧化钠溶液中滴加3滴酚酞溶液,再向该溶液中逐滴加入稀盐酸;观察到溶液由红色变为无色. | 该反应的实质是氢离子和氢氧根离子结合成水分子 | 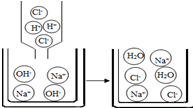 |
5.比较推理是化学学习中常用的思维方法,下列推理正确的是( )
| A. | 生铁比纯铁硬,故黄铜比纯铜硬 | |
| B. | CO有毒,故CO2也有毒 | |
| C. | 金刚石很硬,故石墨也很硬 | |
| D. | 氢氧化铝可治疗胃酸过多,故氢氧化钠也可治疗胃酸过多 |
12.下列物质都属于纯净物的一组是( )
①冰水混合物 ②洁净的空气 ③氧气 ④石灰水.
①冰水混合物 ②洁净的空气 ③氧气 ④石灰水.
| A. | ①③ | B. | ②④ | C. | ①② | D. | ③④ |
2.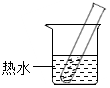 如表是KNO3在不同温度时的溶解度,请回答下列问题.
如表是KNO3在不同温度时的溶解度,请回答下列问题.
(1)20℃时,在装有5g KNO3晶体的试管中,加入10g水并充分振荡,此时所得溶液为饱和(选填“饱和”或“不饱和”)溶液.
(2)将该试管放入盛有热水的烧杯中,使试管内溶液温度升至40℃,此时试管内的溶液中溶剂与溶质的质量比为2:1.
(3)20℃时,不能(填“能”或“不能”)配制溶质质量分数为31.6%的KNO3溶液.
(4)60℃时,100gKNO3饱和溶液,恒温蒸发10g水后,可析出KNO3的质量为11g.
 如表是KNO3在不同温度时的溶解度,请回答下列问题.
如表是KNO3在不同温度时的溶解度,请回答下列问题.| 温度℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度(g) | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)将该试管放入盛有热水的烧杯中,使试管内溶液温度升至40℃,此时试管内的溶液中溶剂与溶质的质量比为2:1.
(3)20℃时,不能(填“能”或“不能”)配制溶质质量分数为31.6%的KNO3溶液.
(4)60℃时,100gKNO3饱和溶液,恒温蒸发10g水后,可析出KNO3的质量为11g.
 日常生活中接触的金属材料,大多属于合金.其中黄铜是以锌作主要添加元素的铜合金.已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示.试计算:
日常生活中接触的金属材料,大多属于合金.其中黄铜是以锌作主要添加元素的铜合金.已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示.试计算: 太阳能电动车是在电动车的基础上,将太阳能转化成电能对车进行供电的,在很大程度上降低了电动车的使用成本,及时有效地补充电动车野外行驶途中的电量.请回答下列相关问题:
太阳能电动车是在电动车的基础上,将太阳能转化成电能对车进行供电的,在很大程度上降低了电动车的使用成本,及时有效地补充电动车野外行驶途中的电量.请回答下列相关问题: