题目内容
10.如图是 A、B、C 三种物质的溶解度曲线,下列分析正确的是( )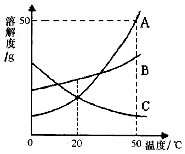
| A. | 20℃时 A、B、C 三种物质的溶解度由大到小的顺序是 A>B>C | |
| B. | 50℃时把 50gA 放入 50g 水中能得到 100gA 的饱和溶液 | |
| C. | 分别将 50℃时 A、B 的饱和溶液降温到 20℃,B 析出的晶体可能比 A 多 | |
| D. | 将 50℃时 A、B、C 三种物质的饱和溶液降温至 20℃时,这三种溶液的溶质质量分数的大小关系是 B>A=C |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、通过分析溶解度曲线可知,20℃时,A、B、C 三种物质的溶解度由大到小的顺序是 B>A=C,故A错误;
B、50℃时,A物质的溶解度是50g,所以把50gA放入50g水中能得到75gA的饱和溶液,故B错误;
C、分别将50℃时A、B 的饱和溶液降温到20℃,如果饱和溶液的质量相等,B析出的晶体比A多,故C正确;
D、20℃时,B物质的溶解度最大,A物质的溶解度次之,降低温度,A、B物质会析出晶体,C物质不会析出晶体,应该按照50℃时的溶解度进行计算,所以将50℃时A、B、C 三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A>C,故D错误.
故选:C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
1.下列选用的除杂试剂和实验操作都正确的是(括号内为杂质)( )
| 选项 | 物质 | 除杂试剂 | 操作方法 |
| A | CO(CO2) | 氢氧化钠溶液 | 气体通过盛有足量氢氧化钠溶液的洗气瓶 |
| B | K2CO3(KCl) | 稀盐酸 | 加入足量稀盐酸、蒸发、结晶 |
| C | FeSO4 (CuSO4) | 锌粉 | 加入足量锌粉并过滤 |
| D | Zn(Fe) | 稀硫酸 | 加入足量的稀硫酸,过滤 |
| A. | A | B. | B | C. | C | D. | D |
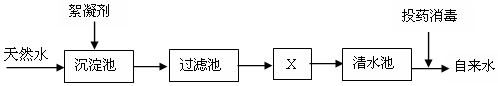
18.下列有关水的知识,其中正确的是( )
| A. | 自然界中的水中大多数为纯净物 | |
| B. | 农业上合理使用化肥和农药有利于水资源的保护 | |
| C. | 只有用蒸馏的方法才能降低水的硬度 | |
| D. | 我国可利用的淡水资源十分丰富 |
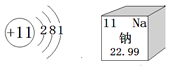
5.下列含氮的物质中,氮元素的化合价最低的是( )
| A. | HNO3 | B. | N2 | C. | NaNO2 | D. | NH3•H2O |
3.实验室学习化学的重要途径,小亮在学习酸碱盐的性质时做了如下实验,请你和他一起完成实验活动.

(1)在白色点滴板上完成实验A,请将实验现象补充完整.
(2)在实验B的烧杯②中滴加2滴酚酞溶液后,扣上大烧杯,一段时间后看到的现象是烧杯②中的溶液由红色变成无色,本实验不仅说明了分子是不断运动的,还说明了盐酸具有挥发性.
(3)在实验C的试管①中,滴加少量的氢氧化钠溶液,看到的现象是产生蓝色沉淀,反应的化学方程式是CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
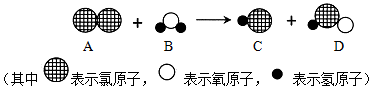
(4)小亮用实验D验证二氧化碳与氢氧化钠溶液反应,看到的现象是气球膨胀.
(5)上述实验验证了碱的4条化学性质.

(1)在白色点滴板上完成实验A,请将实验现象补充完整.
| 实验操作 | 向稀硫酸中滴加石蕊溶液 | 向氢氧化钙溶液中滴加石蕊溶液 |
| 实验现象 | 溶液变红色 | 溶液变蓝色 |
(3)在实验C的试管①中,滴加少量的氢氧化钠溶液,看到的现象是产生蓝色沉淀,反应的化学方程式是CuSO4+2NaOH=Na2SO4+Cu(OH)2↓.
(4)小亮用实验D验证二氧化碳与氢氧化钠溶液反应,看到的现象是气球膨胀.
(5)上述实验验证了碱的4条化学性质.
8.配制50g溶质的质量分数为10%的氯化钠溶液,不需要的仪器是( )
| A. | 量筒 | B. | 烧杯 | C. | 铁架台 | D. | 天平 |