题目内容
15.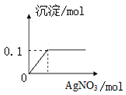 欲测定实验室一瓶久置NaCl溶液的质量分数.取117.0g待测溶液,向其中逐滴加入足量AgNO3溶液,产生沉淀的物质的量与所加硝酸银物质的量的关系如图所示.
欲测定实验室一瓶久置NaCl溶液的质量分数.取117.0g待测溶液,向其中逐滴加入足量AgNO3溶液,产生沉淀的物质的量与所加硝酸银物质的量的关系如图所示.(1)所得沉淀的质量是14.35g(保留0.01g).
(2)求待测溶液中NaCl的质量分数5.0%(根据化学方程式列式计算).
分析 由于题目给出了生成的氯化银的物质的量,所以根据氯化银的物质的量求算质量和根据化学方程式求算氯化钠的质量,进而求算对应溶液中氯化钠的质量分数
解答 解:
(1)由于生成的氯化银的物质的量为0.1mol
所以氯化银的质量为0.1mol×143.5g/mol=14.35g;
(2)设待测液中含氯化钠的质量为x
NaCl+AgNO3=2NaNO3+AgCl↓
58.5 143.5
x 14.35g
$\frac{58.5}{143.5}$=$\frac{x}{14.35g}$
x=5.85g
待测液中NaCl的质量分数是$\frac{5.85g}{117.0g}$×100%=5.0%.
答:(1)所得沉淀的质量是 14.35g(保留0.01g).
(2)待测溶液中NaCl的质量分数 5.0%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
7.将下列各组物质按酸、碱、氧化物分类顺次排列,正确的是( )
| A. | 硝酸,烧碱,水 | B. | 盐酸,熟石灰,苛性钠 | ||
| C. | 碳酸,乙醇,生石灰 | D. | 硫酸,纯碱,石灰石 |
6.甲烷与氢气的燃料混合气在燃烧炉内完全燃烧后,炉气成分如表:
若空气中N2与O2的物质的量分数分别为0.79和0.21,计算:
(1)燃料混合气中甲烷与氢气的物质的量之比
(2)燃料混合气与空气的物质的量之比.
| N2 | CO2 | O2 | H2O | |
| 物质的量分数 | 0.7110 | 0.0810 | 0.0225 | 0.1710 |
(1)燃料混合气中甲烷与氢气的物质的量之比
(2)燃料混合气与空气的物质的量之比.
3.铝是地壳中含量最多的金属元素,其元素符号是( )
| A. | Al | B. | Cl | C. | Ag | D. | Si |
10.对实验现象和结论描述均正确的是( )
| A. | 打开浓盐酸瓶口产生白烟,说明浓盐酸有挥发性 | |
| B. | 稀盐酸中滴入紫色石蕊试液,溶液变红,说明酸遇指示剂变色 | |
| C. | 滴有品红的水呈红色,通过活性炭后变无色,说明活性炭具有吸附性 | |
| D. | 硫在空气中燃烧发出蓝紫色火焰,说明硫具有可燃性 |
20.我国自主研发的抗肿瘤新药西达苯胺(化学式是C22H19FN4O2,相对分子质量为390.4),填补了我国T细胞淋巴瘤新药的空白.下列说法正确的是( )
| A. | 西达苯胺由五种元素构成 | |
| B. | 一个西达苯胺分子的质量是390.4g | |
| C. | 西达苯胺中氮元素的质量分数14.3% | |
| D. | 西达苯胺由48个原子构成 |
7.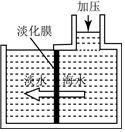 海水淡化可采用膜分离技术.如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中其他各种离子不能通过淡水膜,从而得到淡水.下列说法正确的是( )
海水淡化可采用膜分离技术.如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中其他各种离子不能通过淡水膜,从而得到淡水.下列说法正确的是( )
 海水淡化可采用膜分离技术.如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中其他各种离子不能通过淡水膜,从而得到淡水.下列说法正确的是( )
海水淡化可采用膜分离技术.如图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中其他各种离子不能通过淡水膜,从而得到淡水.下列说法正确的是( )| A. | 淡化膜可以换成滤纸 | B. | 右侧溶剂质量减少 | ||
| C. | 左侧溶液质量不变 | D. | 右侧溶质质量分数减少 |
4.下列碳和碳的化合物的说法正确的是( )
| A. | 金刚石、石墨均是碳元素的单质,两者混在一起属于纯净物 | |
| B. | CO、CO2都有毒,都是大气污染物 | |
| C. | 活性炭、木炭能与空气或水中的杂质发生反应,有吸附性 | |
| D. | 甲烷(CH4)、乙醇(C2H5OH)都含碳元素,都属于有机物 |
5.以甲为原料合成化工产品丁的微观过程如图.下列说法正确的是( )
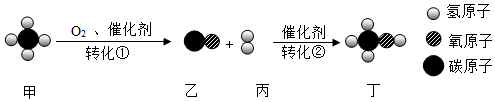

| A. | 乙、丁为氧化物 | B. | 转化①中乙和丙的质量之比为28:2 | ||
| C. | 甲中的氢元素质量分数小于丁中 | D. | 转化②为化合反应 |