题目内容
7. 实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里.由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【理论分析】为了确定该溶液,他们首先进行了分析:
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠溶液.
(2)乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1.
设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
| 实 验 操 作 | 实 验 现 象 |
| ①取少量该无色溶液于试管中,慢慢滴加BaCl2溶液. ②静置后,倾去上层清液,向沉淀中滴加稀盐酸. | 产生白色沉淀. 产生大量气泡,沉淀消失. |
(3)该瓶无色溶液的溶质是碳酸钠.生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(4)丙同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
| 实 验 操 作 | 实 验 现 象 |
分析 根据缺损标签的有关元素组成以及物质的性质来推断试剂的成分,碳酸盐能与盐酸反应生成二氧化碳气体,据此解答即可.
解答 解:(1)氯化钠是由钠元素和氯元素组成的,不含有氧元素,故一定不会是氯化钠溶液,故填:氯化钠;
(2)此标签中钠元素右下角的数字为2,而碳酸氢钠的化学式为NaHCO3,硝酸钠的化学式为NaNO3,故不会是碳酸氢钠和硝酸钠,故填:碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1;
(3)硫酸钠能与氯化钡反应生成硫酸钡沉淀,但是硫酸钡沉淀不溶于盐酸,滴加盐酸不会出现溶解的情况,故不会是硫酸钠;碳酸钠与氯化钡湖反应生成碳酸钡沉淀,碳酸钡沉淀能溶于盐酸且产生气体,故该瓶溶液是碳酸钠溶液,故填:碳酸钠,Na2CO3+BaCl2=BaCO3↓+2NaCl;
(4)碳酸钠能与盐酸反应生成二氧化碳气体,而硫酸钠不能与盐酸反应,故可以直接向溶液中加入盐酸,观察是否产生气泡,故填:
| 实验步骤 | 实验现象 | 结论 |
| 取上述无色溶液少许于试管中,滴加少量的稀盐酸 | 溶液中没有气泡产生(或有气泡产生) | 该瓶无色溶液是硫酸钠溶液(或碳酸钠溶液) |
点评 本题考查了破损标签瓶中试剂的确定,完成此题,可以依据破损标签中所含有的元素以及有关物质的性质进行分析及设计实验.

练习册系列答案
相关题目
17.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色,有关判断正确的是( )
| A. | 滤渣中一定有银、没有铜和锌 | |
| B. | 滤渣中一定有银和锌,可能有铜 | |
| C. | 滤液中一定有硝酸锌、硝酸铜、硝酸银 | |
| D. | 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银 |
18.下列实验操作正确的是( )
| A. | 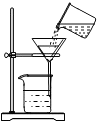 过滤 | B. |  测溶液的pH | C. | 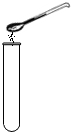 加固体药品 | D. | 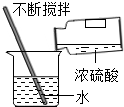 稀释浓硫酸 |
15.下列有关概念应用的判断正确的是( )
| A. | CO2、Fe2O3、H2SO3、O2等都含氧元素,都属于氧化物 | |
| B. | 可燃物与氧气发生的氧化反应都属于燃烧反应 | |
| C. | 生铁和钢都与铁的性质有所不同,都属含碳量不同的铁合金 | |
| D. | 凡是生成盐和水的化学反应都是中和反应 |
12.下列物质的名称、俗称、化学式、物质分类完全对应的是( )
| A. | 汞 水银 Hg 化合物 | |
| B. | 碳酸氢钠 苏打 NaHCO3 盐 | |
| C. | 过氧化氢 双氧水 H2O2 氧化物 | |
| D. | 固态二氧化碳 干冰 CO2 有机物 |
16.麻黄碱可用于治疗支气管哮喘、鼻黏膜充血引起的鼻塞等.它的化学式为C10H15ON,下列说法正确的是( )
| A. | 麻黄碱的相对分子质量为165 | |
| B. | 麻黄碱中含有10个碳原子 | |
| C. | 麻黄碱中氢元素的质量分数最大 | |
| D. | 麻黄碱中氮元素与氧元素的质量比1:1 |
17.锂电池是新型的高能电池,质量轻、电容量大,颇受手机、电脑等用户的青睐.某种锂电池的总反应可表示为Li+MnO2=LiMnO2.以下说法错误的是( )
| A. | 该反应中Li的化合价发生了变化 | B. | MnO2中锰元素的化合价为+4价 | ||
| C. | LiMnO2属于氧化物 | D. | 该反应属于化合反应 |