题目内容
18.下表为氯化钠与碳酸钠在不同温度下的溶解度,下列说法正确者( )| 温度 | 10℃ | 20℃ | 30℃ | 40℃ | |
| 溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸钠 | 12.2 | 21.8 | 39.7 | 49.6 | |
| A. | 20℃时,将100g水加入30g碳酸钠中,充分搅拌后得到不饱和溶液 | |
| B. | 两物质的溶解度曲线在20℃~30℃之间应出现交点 | |
| C. | 可以采用降温结晶的方法从二者的混合物中提纯氯化钠 | |
| D. | 20℃时,将100g水加入30g氯化钠中,充分搅拌后所得溶液中溶质质量分数为到30% |
分析 A、根据20℃时碳酸钠的溶解度考虑;B、根据图表中数据分析;C、根据氯化钠的溶解度受温度影响考虑;D、根据20℃时氯化钠的溶解度考虑.
解答 解:A、20℃时碳酸钠的溶解度是21.8g,所以20℃时,将100g水加入30g碳酸钠中,充分搅拌后得到饱和溶液,故A错;
B、由图表中数据分析,可知两物质的溶解度曲线在20℃~30℃之间有相等的可能,应出现交点,故B正确;
C、氯化钠的溶解度受温度影响较小,用蒸发溶剂的方法提纯,故C错;
D、20℃时氯化钠的溶解度是36g,所以20℃时,将100g水加入30g氯化钠中得到不饱和溶液,溶质质量分数不等于30%,故D错.
故选B.
点评 解答本体关键是熟悉溶解度的四要素,并能灵活运用解决实际问题.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案
相关题目
7.为检验某混合气体成分做了如下实验:将一定体积的该混合气体通过过量的澄清石灰水,石灰水无明显现象,气体总体积减小,把剩余气体导出后,可在氧气中燃烧,燃烧产物能使白色CuSO4粉末变蓝色,则原混合气体的成分可能是( )
| A. | CO2和CO | B. | HCl和H2 | C. | CH4和CO2 | D. | HCl和CO |
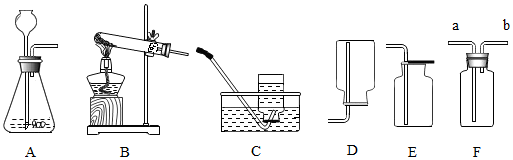
8.下列实验设计错误的是( )
| A. | 用蒸馏的方法可以使硬水软化 | B. | 用湿润的红色石蕊试纸检验NH3 | ||
| C. | 用灼热的铜网除去N2中的O2 | D. | 用100mL量筒量取5.6 mL溶液 |
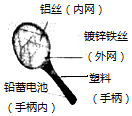 (1)图中标示的材料中含有的金属活动性最弱的是Pb(填符号);属于合成材料的物质是塑料.
(1)图中标示的材料中含有的金属活动性最弱的是Pb(填符号);属于合成材料的物质是塑料.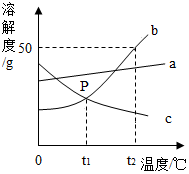 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题: 明末宋应星于崇祯十年(公元1637年)所著《天工开物》,炼锌工艺的现存文字记载:
明末宋应星于崇祯十年(公元1637年)所著《天工开物》,炼锌工艺的现存文字记载: