题目内容
(6分)火力发电厂用石灰石泥浆吸收废气中的二氧化硫以防止污染环境,其反应方程式:2CaCO3+2SO2+O2==2CaSO4+2CO2。
(1)若1000克废气中含1.6克二氧化硫,则处理1000克这种废气需要多少克碳酸钙?
(2)处理上述1000克废气,可得到含85%CaSO4的粗产品多少克?
(1)2.5克(2)4克
【解析】
试题分析:【解析】
设需CaCO3的质量为x,生成纯CaSO4的质量为y。
2CaCO3+2SO2+O2==2CaSO4+2CO2
200 128 272
x 1.6克 y
 x=2.5克
x=2.5克
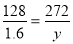 y=3.4克
y=3.4克
3.4克÷85%=4克
考点:根据化学方程式的计算

练习册系列答案
相关题目