题目内容
在托盘天平两盘上,放上A、B两个烧杯,烧杯内均盛有质量不同但都含有硫酸9.8克的稀硫酸,已知A烧杯比B烧杯重,现在A、B两烧杯中分别投入等质量的铁和锌反应结束后,天平保持平衡,则反应前A、B烧杯最大质量差为 或 .
考点:金属的化学性质,根据化学反应方程式的计算
专题:金属与金属材料
分析:根据:氢气的质量=
×金属质量以及金属活动性顺序,推测答案.
| 金属的化合价 |
| 金属的相对原子质量 |
解答:解:根据:氢气的质量=
×金属质量,显然是A烧杯“加铁”放出的氢气必须比B烧杯“加锌”放出的氢气多,即:换句话说就是A烧杯增加的质量必须比B烧杯增加的质量小.而如果“含有硫酸9.8克的稀硫酸”全部参加反应,则放出的氢气一样多,所以B烧杯中,硫酸必须有剩余.
我们先考虑第一种可能:铁过量,锌不足. 设它们都是a克(5.6<a<6.5),则A烧杯增加质量=a-0.2 克,B烧杯增加质量=
克,两烧杯质量增加的差=
克-(a-0.2 克)=0.2-
,把a=6.5代入,得下限值=0克.【此为答案的最小值,应该比它大,不包括它】.
再考虑第二种可能:铁锌都不足,设它们都是a克(a<5.6),则A烧杯增加质量=
克,B烧杯增加质量=
克,两烧杯质量增加的差=
g-
g=
g,把a=5.6代入,得上限值=0.0277克.【此为答案的最大值,应该比它小,不包括它】.
所以,答案应该是反应前AB烧杯质量差为大于0且小于0.0277克,加入的金属质量应该是大于0且小于6.5克.
故答案为:0.0027g,0.0014g.
| 金属的化合价 |
| 金属的相对原子质量 |
我们先考虑第一种可能:铁过量,锌不足. 设它们都是a克(5.6<a<6.5),则A烧杯增加质量=a-0.2 克,B烧杯增加质量=
| 63a |
| 65 |
| 63a |
| 65 |
| 2a |
| 65 |
再考虑第二种可能:铁锌都不足,设它们都是a克(a<5.6),则A烧杯增加质量=
| 54a |
| 56 |
| 63a |
| 65 |
| 63a |
| 65 |
| 54a |
| 56 |
| 9a |
| 1820 |
所以,答案应该是反应前AB烧杯质量差为大于0且小于0.0277克,加入的金属质量应该是大于0且小于6.5克.
故答案为:0.0027g,0.0014g.
点评:根据氢气的质量=
×金属质量以及金属活动性顺序,进行处理.
| 金属的化合价 |
| 金属的相对原子质量 |

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目

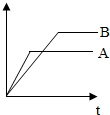 等质量的A、B两种金属,分别与相同且足量的稀盐酸反应(已知A、B在生成物分别为ACl2 BCl2)生成H2的质量和反应时间关系如图,请回答:
等质量的A、B两种金属,分别与相同且足量的稀盐酸反应(已知A、B在生成物分别为ACl2 BCl2)生成H2的质量和反应时间关系如图,请回答: