题目内容
4.某兴趣小组为了测定铜锌合金(不含其它杂质)中锌的质量分数.取10g合金样品放入试管中,加入足量稀硫酸充分反应后,溶液中还剩余部分固体,试管中物质总质量减少0.1g.请回答:(1)溶液中剩余固体成分是铜.
(2)试管中物质总质量减少0.1g,是因为生成了氢气.
(3)样品中锌的质量是3.25gg.
(4)样品中锌的质量分数是32.5%.
分析 根据金属活动性顺序可知,铜锌合金中的锌能与稀硫酸反应,铜不反应,由于稀硫酸是足量的,溶液中剩余固体成分是铜.由质量守恒定律可知,试管中物质总质量减少的质量就是生成氢气的质量,根据锌与硫酸反应的方程式,由氢气的质量求出锌的质量,进而求出样品中锌的质量分数.
解答 解:
(1)由题意及金属活动性顺序可知,铜锌合金中的锌能与稀硫酸反应,铜不反应,溶液中剩余固体成分是铜;
(2)由质量守恒定律可知,试管中物质总质量减少0.1g,是因为生成了氢气;
(3)设样品中锌的质量是X
Zn+H2SO4═ZnSO4+H2↑
65 2
X 0.1g
$\frac{65}{X}=\frac{2}{0.1g}$
解得:X=3.25g
(4)样品中锌的质量分数是:$\frac{3.25g}{10g}$×100%=32.5%
故答案为:(1)铜;(2)氢气;(3)3.25g;(4)32.5.
点评 本题主要考查学生判断物质间的反应关系以及运用化学方程式进行计算的能力.学生需认真分析反应关系,正确书写化学方程式,才能解决

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
14.下列用分子的观点对生活中现象或事实的解释不正确的是( )
| A. | 擦黑板时粉尘飞扬-分子在不断运动 | |
| B. | 温度计中的水银热胀冷缩-分子间间隔改变 | |
| C. | CO和CO2的化学性质不同-分子构成不同 | |
| D. | 湿衣服在阳光下比在阴凉处干得快-温度越高,分子运动速率越快 |
12.下列化学方程式书写正确的是( )
| A. | 2P+5O2═2P2O5 | B. | C+O2═CO2↑ | ||
| C. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | D. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 |
16.氧化汞受热时的变化可用如图表示(图中大圆圈表示汞原子,小圆圈表示氧原子).据图得出的错误结论是( )
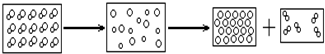

| A. | 氧化汞受热时能分解成汞和氧气 | |
| B. | 原子是化学变化中的最小粒子 | |
| C. | 原子是不能再分的粒子 | |
| D. | 化学反应的实质是分子的再分和原子的重新组合 |
13.下列关于氧气的说法,正确的是( )
| A. | 灯泡中填充氧气可以延长其使用寿命 | |
| B. | 用含有氧元素的物质反应才有可能产生氧气 | |
| C. | 鱼、虾等能在水中生存,是由于氧气极易溶于水 | |
| D. | 测定空气中氧气含量的实验可以将红磷换成蜡烛 |
14.下列鉴别物质的试剂或方法,不正确的是( )
| 选项 | 待鉴别的物质 | 鉴别试剂或方法 |
| A | 氯化钾与氯化铵 | 熟石灰、研磨 |
| B | 硝酸铵与食盐 | 水 |
| C | 氮气与二氧化碳 | 点燃的木条 |
| D | 一氧化碳与二氧化碳气体 | 澄清的石灰水 |
| A. | A | B. | B | C. | C | D. | D |
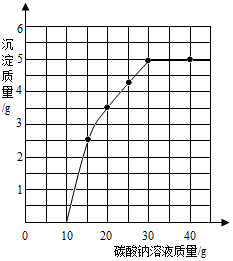 实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.
实验室用过量的稀盐酸和大理石制取CO2,取50g反应后的滤液,逐滴滴入碳酸钠溶液,测得滴入碳酸钠溶液的质量与产生沉淀质量的关系曲线如图所示.