题目内容
14.向盛有100g质量分数为4.9%的硫酸的烧杯中逐滴滴入质量分数为4%的NaOH溶液,下列表示烧杯中溶液的pH、导电性及溶液中质量分数的变化情况(注图中横坐标均表示所加NaOH溶液的质量m),图象正确的是( )| A. | 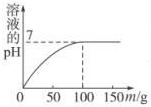 | B. |  | ||
| C. |  | D. | 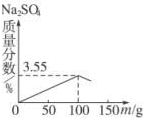 |
分析 A、根据氢氧化钠和硫酸反应完全后,继续滴加氢氧化钠,溶液的pH值将大于7进行分析;
B、根据硫酸和氢氧化钠反应生成硫酸钠和水,恰好完全反应时,溶液中含有钠离子、硫酸根离子,导电性不会为零进行分析;
CD、根据氢氧化钠和硫酸反应生成硫酸钠和水,然后结合题中的数据和图象进行分析.
解答 解:A、氢氧化钠和硫酸反应完全后,继续滴加氢氧化钠,溶液的pH值将大于7,不会变成水平线,故A错误;
B、硫酸和氢氧化钠反应生成硫酸钠和水,恰好完全反应时,溶液中含有钠离子、硫酸根离子,导电性不会为零,故B错误;
C、H2SO4+2NaOH═2H2O+Na2SO4
98 80 142
100g×4.9% y z
$\frac{98}{100g×4.9%}$=$\frac{80}{y}$=$\frac{142}{z}$
所以y=4g,z=7.1g
$\frac{4g}{4%}$=100g
当氢氧化钠质量为100g时,恰好完全反应,生成硫酸钠的质量分数为:$\frac{7.1g}{200g}$×100%=3.55%,故C错误;
D、通过分析硫酸钠的质量分数为:$\frac{7.1g}{200g}$×100%=3.55%,故D正确.
故选:D.
点评 本题是多个知识点的考查题,能对多个物质的反应过程达到有效分析,并能结合读懂图象是解题的关键.

练习册系列答案
相关题目
5.下列关于碳的性质的叙述中正确的是( )
| A. | 碳单质不都是黑色的固体 | |
| B. | 碳在高温下只能还原金属氧化物 | |
| C. | 碳的化学性质很活泼,易与空气中的氧气反应 | |
| D. | 碳和氧气在点燃条件下反应,生成CO时需要吸收热量 |
2.氢氧化钠中含有碳酸钠,请写出能证明含有碳酸钠的两种方法,写出试剂的化学式(提示碳酸钠溶液显碱性):HCl、Ca(OH)2,
请选其中的一种完成下列实验报告:
请选其中的一种完成下列实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样品粉末,加入适量的水配成溶液,加入澄清的石灰水 | 出现浑浊沉淀 | 证明含有碳酸钠 |
3.除去下列各物质中的少量杂质所选用的试剂及操作方法均正确的是( )
| 选项 | 物质 | 杂质(少量) | 试剂 | 操作方法 |
| A | KNO3 | MnO2 | 足量的水 | 溶解、过滤、蒸发 |
| B | H2 | 水蒸气 | 适量的NaOH溶液 | 洗气 |
| C | 硝酸 | 盐酸 | 过量的硝酸银溶液 | 过滤 |
| D | CaO | CaCO3 | 足量的水 | 溶解、过滤 |
| A. | A | B. | B | C. | C | D. | D |
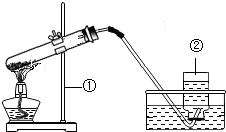 如图是实验室用氯酸钾和二氧化锰制取和收集氧气的装置,回答下列问题:
如图是实验室用氯酸钾和二氧化锰制取和收集氧气的装置,回答下列问题: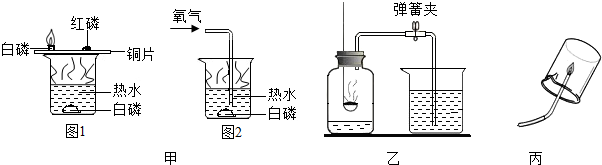

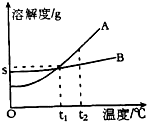 A、B两物质的溶解度曲线如图所示,请根据曲线回答下列问题:
A、B两物质的溶解度曲线如图所示,请根据曲线回答下列问题: