题目内容
一定质量的甲烷在不充足的氧气中燃烧,甲烷完全反应,生成CO、CO2、H2O的总质量为10.4 g,若其中H2O的质量为5.4 g,计算生成CO的质量。
解法一:
解:设生成CO的CH4的质量为x,生成CO2的CH4的质量为y。
CH4 ~ CO ~ 2H2O CH4 ~ CO2 ~ 2H2O
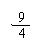
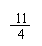
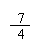
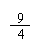 16
16  28 36 16 44 36
28 36 16 44 36
x x× x× y y× y×
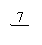 | |||
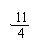 | |||
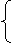 x× +y× = 5 g
x× +y× = 5 g
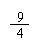
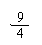
x× +y× = 5.4 g
x=1.6 g

1.6 g× =2.8 g
解法二:
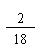 甲烷中的C:H的质量比为3:1
甲烷中的C:H的质量比为3:1
生成物中氧元素的质量:10.4 g-5.4 g× ×4=8 g
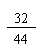

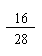 设一氧化碳的质量为x,则:
设一氧化碳的质量为x,则:
×x+( 10.4 g-5.4 g-x)× +5.4 g× =8 g x=2.8 g
解法三:碳元素的质量为1.8 g
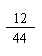
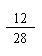 设一氧化碳的质量为x,则: ×x+(10.4 g-5.4 g-x)× =1.8 g
设一氧化碳的质量为x,则: ×x+(10.4 g-5.4 g-x)× =1.8 g
x=2.8 g

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目