题目内容
19.由于高铁列车车厢是密闭的空间,因此提供清洁的空气、保持车厢的卫生非常重要.(1)高铁酸钠(Na2FeO4)是高铁上常用的一种“绿色环保高效”消毒剂.
①高铁酸钠中铁元素的化合价为+6;
②下面是一种制备高铁酸钠的反应原理:Fe2O3+3NaNO3+4NaOH═2Na2FeO4+3NaNO2+2X,X的化学式为H2O.
(2)某品牌的空气净化剂含有过氧化钠(Na2O2),它可以使车厢里的二氧化碳转化为碳酸钠和氧气,写出其化学反应方程式2Na2O2+2CO2=2Na2CO3+O2.
分析 (1)①根据在化合物中正负化合价代数和为零,结合高铁酸钠的化学式进行解答即可.
②由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
(2)过氧化钠与车厢里的二氧化碳转化为碳酸钠和氧气,写出反应的化学方程式即可.
解答 解:(1)①钠元素显+1价,氧元素显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6价.
②由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式Fe2O3+3NaNO3+4NaOH═2Na2FeO4+3NaNO2+2X,反应前铁、氧、钠、氮、氢原子个数分别为2、16、7、3、4,反应后的生成物中铁、氧、钠、氮、氢原子个数分别为2、14、7、3、0,根据反应前后原子种类、数目不变,则2X分子中含有2个氧原子和4个氢原子,则每个X分子由1个氧原子和2个氢原子构成,则物质X的化学式为H2O.
(2)过氧化钠与车厢里的二氧化碳转化为碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2.
故答案为:(1)①+6;②H2O;(2)2Na2O2+2CO2=2Na2CO3+O2.
点评 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、化学反应前后原子守恒来确定物质的化学式、化学方程式的书写方法即可正确解答此类题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.“低碳生活“是指减少能源消耗,节约资源,从而减少CO2排放的生活方式,下列不符合”低碳生活“的做法或理念是( )
| A. | 使用节能灯泡 | |
| B. | 近距离出行用自行车代替机动车 | |
| C. | 大力兴建火力发电站以解决人们对电力的需求 | |
| D. | 更多地利用太阳能等能源 |
7.下列有关合金的叙述正确的是( )
①合金至少含有两种金属
②合金中的元素以化合物的形式存在
③合金中一定含有金属元素
④合金一定是混合物
⑤生铁是含少量杂质的铁合金
⑥生铁可完全溶解于稀盐酸中.
①合金至少含有两种金属
②合金中的元素以化合物的形式存在
③合金中一定含有金属元素
④合金一定是混合物
⑤生铁是含少量杂质的铁合金
⑥生铁可完全溶解于稀盐酸中.
| A. | ①②③④⑤⑥ | B. | ①②③ | C. | ③④⑤ | D. | ④⑤⑥ |
4.对下列物质的归类正确的是( )
| A. | 盐酸、冰水共存物--混合物 | B. | 水、干冰--单质 | ||
| C. | 塑料、合成橡胶--有机合成材料 | D. | 纯碱、烧碱--碱 |
9.如图为某微观反应过程,
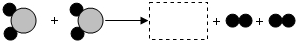
(1)该反应为分解反应(填反应类型).
(2)虚线框内应填的为D,你所选择的依据为质量守恒定律(或化学反应前后原子种类、数目不变).
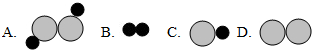
(3)在一密闭容器中有M、N、P、Q四种物质,在一定条件下使之充分反应后,测得反应前后各物质的质量如表所示:
则N的待测值为18.

(1)该反应为分解反应(填反应类型).
(2)虚线框内应填的为D,你所选择的依据为质量守恒定律(或化学反应前后原子种类、数目不变).
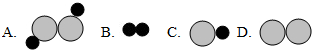
(3)在一密闭容器中有M、N、P、Q四种物质,在一定条件下使之充分反应后,测得反应前后各物质的质量如表所示:
| 物质 | M | N | P | Q |
| 反应前的质量/g | 80 | 1 | 1 | 1 |
| 反应后的质量/g | 1 | 待测 | 45 | 19 |