题目内容
8.有一Fe和FeO的混合物7.0g,与100克9.8%的稀硫酸取恰好完全反应,则生成硫酸亚铁的质量为( )| A. | 7.6g | B. | 15.2g | C. | 20.0g | D. | 40.0g |
分析 根据已有的知识进行,Fe和FeO的混合物与硫酸反应生成硫酸亚铁,可以根据质量守恒定律,根据硫酸的质量即可求出生成硫酸亚铁的质量.
解答 解:铁与氧化亚铁的混合物,与100克9.8%的稀硫酸取恰好完全反应,FeO+H2SO4═FeSO4+H2O;Fe+H2SO4═FeSO4+H2↑;
设生成硫酸亚铁的质量为x,
H2SO4~FeSO4
98 152
100g×9.8% x
$\frac{98}{100g×9.8%}=\frac{152}{x}$
x=15.2g
故答案为:B.
点评 本题主要考查了质量守恒定律方面的内容或根据化学方程式的计算,完成此题,也可以依据反应的化学方程式结合题干提供的数据进行.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
13.金刚石、石墨和C60都是由碳元素组成的单质,下列说法正确的是( )
| A. | 它们是同一种物质 | B. | 它们碳原子排列方式相同 | ||
| C. | 金刚石硬度大,可用它切割大理石 | D. | 它们的物理性质相同 |
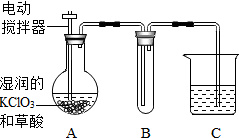 2013年12月,杭州、萧山等地不少市民曾反映,自来水里有股奇怪的味道,一些市民怀疑是自来水厂往自来水中通入了过量的氯气.经浙江省和沿岸地市环保部门对钱塘江全流域开展的排查,异味来自于钱塘江沿岸企业所排放的一种叫邻叔丁基苯酚的物质.其实,世界环保联盟建议全面禁止用氯气对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2,ClO2是一种黄绿色、有刺激性气味的气体,冷却至11.0℃以下时变成红色液体.易溶于水,见光易分解,易与碱反应,杀菌、漂白能力均优于氯气.
2013年12月,杭州、萧山等地不少市民曾反映,自来水里有股奇怪的味道,一些市民怀疑是自来水厂往自来水中通入了过量的氯气.经浙江省和沿岸地市环保部门对钱塘江全流域开展的排查,异味来自于钱塘江沿岸企业所排放的一种叫邻叔丁基苯酚的物质.其实,世界环保联盟建议全面禁止用氯气对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2,ClO2是一种黄绿色、有刺激性气味的气体,冷却至11.0℃以下时变成红色液体.易溶于水,见光易分解,易与碱反应,杀菌、漂白能力均优于氯气.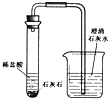 在盛有少量石灰石的试管里加入适量稀盐酸,并将导管的一段伸入装有澄清石灰石的烧杯中,依据实验回答下列问题:
在盛有少量石灰石的试管里加入适量稀盐酸,并将导管的一段伸入装有澄清石灰石的烧杯中,依据实验回答下列问题: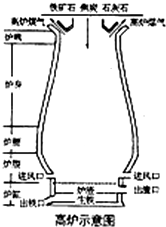 早在春秋战国时期,我国就开始生产和使用铁器.公元1世纪时,铁在我国已经广泛使用.如图为工业炼铁的主要设备--高炉.请你回答下列问题:
早在春秋战国时期,我国就开始生产和使用铁器.公元1世纪时,铁在我国已经广泛使用.如图为工业炼铁的主要设备--高炉.请你回答下列问题: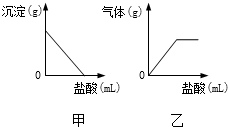 有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH 中的一种或几种.取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加盐酸,沉淀的量、产生气体的量与加入盐酸体积的关系如右图甲、乙所示.
有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH 中的一种或几种.取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加盐酸,沉淀的量、产生气体的量与加入盐酸体积的关系如右图甲、乙所示.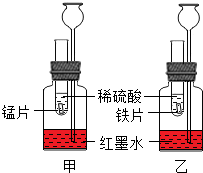 在室温条件下进行如图所示实验.试管内的锰片和铁片表面均被打磨洁净,且形状、大小相同,同时加入等质量和等质量分数的稀硫酸.
在室温条件下进行如图所示实验.试管内的锰片和铁片表面均被打磨洁净,且形状、大小相同,同时加入等质量和等质量分数的稀硫酸.