题目内容
11.在反应2A+B═2C+D 中,5.6g A与7.3g B恰好完全反应生成12.7g C,现要得到0.6g D,则需要A的质量为( )| A. | 5.6g | B. | 16.8g | C. | 21.9g | D. | 无法计算 |
分析 化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和.
化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答 解:设需要A的质量为x,
5.6gA与7.3gB恰好完全反应生成12.7gC,同时生成D的质量为:5.6g+7.3g-12.7g=0.2g,
即反应过程中A和D的质量比是56:2,
2A+B═2C+D,
56 2
x 0.6g
$\frac{56}{x}$=$\frac{2}{0.6g}$,
x=16.8g,
故选:B.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
2.下列区分物质的方法错误的是( )
| A. | 用加碘食盐水区分奶粉和淀粉 | |
| B. | 用高锰酸钾溶液区分二氧化碳和二氧化硫 | |
| C. | 用水鉴别NH4NO3和NaOH固体 | |
| D. | 用点燃闻气味的方法区分羊毛纤维和合成纤维 |
19.现将一定量的铁粉加入盛有Cu(NO3)2、AgNO3混合溶液的烧杯中,充分反应后加入稀盐酸,发现没有气泡但出现白色沉淀,则加入盐酸前的烧杯中可能含有( )
| A. | Fe、AgNO3、Cu(NO3)2、Fe(NO3)2 | B. | Cu、AgNO3、Cu(NO3)2、Fe(NO3)2 | ||
| C. | Ag、AgNO3、Cu(NO3)2、Fe(NO3)2 | D. | Cu、Ag、AgNO3、Fe(NO3)2 |
14.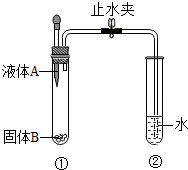 某兴趣小组设计的小实验,装置如图所示.打开止水夹,将A滴入试管①中,A与B接触后,在试管②中的导管口处观察到有气泡冒出.下列液体A和固体B的组合不可能出现上述现象的是( )
某兴趣小组设计的小实验,装置如图所示.打开止水夹,将A滴入试管①中,A与B接触后,在试管②中的导管口处观察到有气泡冒出.下列液体A和固体B的组合不可能出现上述现象的是( )
 某兴趣小组设计的小实验,装置如图所示.打开止水夹,将A滴入试管①中,A与B接触后,在试管②中的导管口处观察到有气泡冒出.下列液体A和固体B的组合不可能出现上述现象的是( )
某兴趣小组设计的小实验,装置如图所示.打开止水夹,将A滴入试管①中,A与B接触后,在试管②中的导管口处观察到有气泡冒出.下列液体A和固体B的组合不可能出现上述现象的是( )| A. | 水和烧碱 | B. | 稀硫酸和镁条 | C. | 稀盐酸和小苏打 | D. | 水和硝酸铵 |
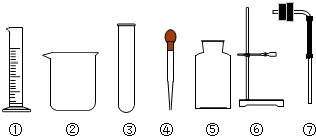 实验桌上摆放有下列仪器,请按下列要求填写下列空白.
实验桌上摆放有下列仪器,请按下列要求填写下列空白.