题目内容
19.下列叙述正确的是( )| A. | 4g氢气和8g氧气混合,点燃充分反应生成12g水 | |
| B. | 3g木炭在空气中完全燃烧,生成11 g二氧化碳,参加反应的氧气的质量为8g | |
| C. | 煤燃烧后,煤与氧气的质量总和与生成的气体的质量相等 | |
| D. | 镁条在空气里燃烧,生成的氧化镁的质量一定大于镁条的质量 |
分析 化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和.
解答 解:A、氢气燃烧的化学方程式及其反应物、生成物之间的质量比为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,
4 32 36
由反应物、生成物之间的质量比可知,1g氢气和8g氧气恰好完全反应生成9g水,该选项叙述不正确;
B、木炭燃烧的化学方程式及其反应物、生成物之间的质量比为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,
12 32 44
由反应物、生成物之间的质量比可知,3g木炭在8g氧气中完全燃烧,能生成11g二氧化碳,该选项叙述正确;
C、煤燃烧是煤与空气中的氧气反应,煤中的一些杂质不反应,根据质量守恒定律,煤与氧气的质量总和与生成的气体质量不相等,该选项叙述不正确;
D、镁带在空气中燃烧,是镁与空气中的氧气反应,根据质量守恒定律,镁与参加反应的空气中的氧气的质量应等于生成的氧化镁的质量,因此生成的氧化镁的质量一定大于镁带的质量,该选项叙述正确;
故选:BD.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.

练习册系列答案
相关题目
18.月球上的“氦-3”蕴藏量巨大,探月的目的之一是获取核聚变燃料──氦-3,以解决地球能源危机.氦-3原子核里有2个质子,1个中子,相对原子质量为3,下列表示氦-3原子的结构示意图中正确的是( )
| A. | 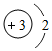 | B. |  | C. | 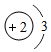 | D. | 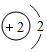 |
19.能源问题是当今世界三大问题之一,下列有关能源的叙述中不正确的是( )
| A. | 乙醇汽油中添加的乙醇属于可再生能源 | |
| B. | 氢气作为能源具有来源广、热值高、无污染等优点,目前氢能已得到大规模的应用 | |
| C. | 将煤球制成“蜂窝煤”是为了增大与空气的接触面积,使其燃烧更充分 | |
| D. | 我国南海海底储藏了大量“可燃冰”,它将成为未来重要的能源 |
14.置换反应是化学反应的基本类型之一.金属与盐溶液之间的置换反应,一般是活动性较强的金属可把活动性较弱的金属从其盐溶液中置换出来.非金属单质也具有类似金属与盐溶液之间的置换反应规律,即活动性较强的非金属可把活动性较弱的非金属从其盐溶液中置换出来,如在溶液中可发生下列反应:
C12+2NaBr=2NaCl+Br2; Br2+2KI=2KBr+I2; I2+Na2S=2NaI+S↓
由此可判断下列化学方程式书写错误的是( )
C12+2NaBr=2NaCl+Br2; Br2+2KI=2KBr+I2; I2+Na2S=2NaI+S↓
由此可判断下列化学方程式书写错误的是( )
| A. | C12+2NaI=2NaCl+I2 | B. | I2+2KBr=2KI+Br2 | ||
| C. | Br2+Na2S=2NaBr+S↓ | D. | C12+K2S=2KCl+S↓ |
4.下列有关铁的叙述,错误的是( )
| A. | 生铁含碳量比钢要少 | B. | 铁可以在氧气中燃烧 | ||
| C. | 铁跟盐酸反应生成氯化亚铁和氢气 | D. | 铁在潮湿的空气中会生锈 |
11.下列变化属于化学变化的是( )
| A. | 瓷碗破碎 | B. | 水的蒸发 | C. | 灯泡发光 | D. | 纸张燃烧 |
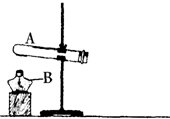 小成同学要在实验室里用高锰酸钾制取氧气.请回答下列问题:
小成同学要在实验室里用高锰酸钾制取氧气.请回答下列问题: