题目内容
鱼苗在长途运输中,通常将鱼苗养在相对密闭的容器内,加入某种药品,使容器内满足下列条件才能保持鱼苗的存活:充足的氧气、及时除去鱼苗呼出的CO2水的pH调节在8左右,碱性不能太强.现有以下四种物质供选择:双氧水、过氧化钙(CaO2).过氧化钠(Na2O2)、氯酸钾.它们的有关化学性质如下:
(1)2H2O2═2H2O+O2↑
(2)2Na2 O2+2H20═4NaOH十O2↑
(3)2Na2O2+2CO2═2Na2CO3+O2
(4)2CaO2+2H2O═2Ca(OH)2+O2↑
(5)2CaO2+2CO2═2CaCO3↓+O2
(6)KClO3不与H2O,CO2反应
在鱼苗长途运输中你认为最适合加入的物质是( )
(1)2H2O2═2H2O+O2↑
(2)2Na2 O2+2H20═4NaOH十O2↑
(3)2Na2O2+2CO2═2Na2CO3+O2
(4)2CaO2+2H2O═2Ca(OH)2+O2↑
(5)2CaO2+2CO2═2CaCO3↓+O2
(6)KClO3不与H2O,CO2反应
在鱼苗长途运输中你认为最适合加入的物质是( )
| A、双氧水 | B、过氧化钙 |
| C、过氧化钠 | D、氯酸钾 |
考点:制取气体的反应原理的探究,常见碱的特性和用途
专题:科学探究
分析:由题意“充足的氧气、鱼苗呼出的二氧化碳要及时除去、为防止细菌繁殖,须将水的pH调节在8左右”,又因为2Ca2O2+2H2O=2Ca(OH)2+O2↑,有氧气生成,且Ca(OH)2在水中的溶解性较弱,相应腐蚀性也小;且2Ca2O2+2CO2=2CaCO3+O2,可以同时消耗二氧化碳,可维持氧气和二氧化碳的平衡;而双氧水虽能制取氧气,但不能消耗二氧化碳;过氧化钠虽能制取氧气,但生成的氢氧化钠为强碱,碱性太强.
解答:解:A、双氧水虽能制取氧气,但不能消耗二氧化碳,故A错误;
B、因为2Ca2O2+2H2O=2Ca(OH)2+O2↑,有氧气生成,且2Ca(OH)2在水中的溶解性较弱,相应腐蚀性也小;且2Ca2O2+2CO2=2CaCO3+O2,可以同时消耗二氧化碳,可维持氧气和二氧化碳的平衡,故B最合适;
C、过氧化钠虽能制取氧气,但生成的碳酸钠为强碱,碱性太强,故C错误;
D、氯酸钾不与H2O,CO2反应,而它需要加热与二氧化锰的条件下,才能进行反应,故D错误.
故选B.
B、因为2Ca2O2+2H2O=2Ca(OH)2+O2↑,有氧气生成,且2Ca(OH)2在水中的溶解性较弱,相应腐蚀性也小;且2Ca2O2+2CO2=2CaCO3+O2,可以同时消耗二氧化碳,可维持氧气和二氧化碳的平衡,故B最合适;
C、过氧化钠虽能制取氧气,但生成的碳酸钠为强碱,碱性太强,故C错误;
D、氯酸钾不与H2O,CO2反应,而它需要加热与二氧化锰的条件下,才能进行反应,故D错误.
故选B.
点评:掌握制取气体的反应原理,熟记常用气体的制取的化学方程式;了解常见碱的特性和用途.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
如图是氢氧化钠溶液与稀硫酸溶液恰好完全反应的微观示意图,由此得出的结论不正确的是( )

| A、反应结束时溶液的pH=7 |
| B、反应前后没有发生变化的微粒是Na+和SO42- |
| C、该反应是Na+和SO42-结合生成Na2SO4 |
| D、该反应的实质是H+和OH-结合生成H2O分子 |
下列取用药品的操作正确的是( )
| A、取用液体药品时,手拿试剂瓶,标签向外,以防腐蚀标签 |
| B、没有指明量,液体取用量需到试管容积的三分之一为宜 |
| C、用胶头滴管代替量筒取2mL的液体 |
| D、取用药品后,及时盖上瓶塞放回原处,标签向外 |
金刚石、石墨和C60都是由碳元素组成的单质,下列关于碳的单质的叙述正确的是( )
| A、都是黑色固体 |
| B、在氧气中充分燃烧时都生成二氧化碳 |
| C、碳原子的排列方式相同 |
| D、一定条件下,石墨转化成金刚石是物理变化 |
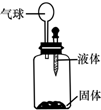 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )①石灰石和稀盐酸 ②镁和稀硫酸 ③碳酸钙固体和水 ④氧化铜和稀硫酸.
| A、①②③④ | B、①② |
| C、①②④ | D、②③④ |