题目内容
在盐酸和氢氧化钠反应的过程中,如图是利用数字化传感器得到的溶液pH变化图象.
(1)反应的化学方程式为 ;
(2)当溶液呈中性时,所消耗氢氧化钠溶液的体积是 mL;
(3)图中b点所示溶液中,含有的溶质是 ;
(4)把两者液体混合时出现了气泡,用方程式表示: .

【考点】中和反应及其应用;溶液的酸碱性与pH值的关系;书写化学方程式、文字表达式、电离方程式.
【专题】常见的酸 酸的通性.
【分析】(1)根据氢氧化钠和盐酸反应生成氯化钠和水书写;
(2)根据图是分析;
(3)b点时,pH>7,溶液显碱性,氢氧化钠过量;
(4)根据把两者液体混合时出现了气泡,可能是氢氧化钠变质解答.
【解答】解:(1)氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:NaOH+HCl=NaCl+H2O;
(2)由图示,当溶液呈中性时,pH=7,此时所消耗氢氧化钠溶液的体积是10ml;
(3)b点时,pH>7,溶液显碱性,氢氧化钠过量,含有的溶质是NaOH和NaCl;
(4)把两者液体混合时出现了气泡,可能是氢氧化钠变质生成碳酸钠,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故答案为:
(1)NaOH+HCl=NaCl+H2O;
(2)10;
(3)NaOH和NaCl;
(4)Na2CO3+2HCl═2NaCl+H2O+CO2↑.
【点评】会正确分析图象是正确解决本题的关键.考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

某同学在化学晚会上用毛笔蘸取一种无色液体在一张白纸上书写了“化学魔术”四字,然后再喷上另一种无色液体,白纸上立即出现了红色的“化学魔术”四字.该同学所用的两种无色液体可能是
|
| A. | NaOH溶液、酚酞溶液 | B. | CuSO4溶液、NaOH溶液 |
|
| C. | 紫色石蕊溶液、酚酞溶液 | D. | 酚酞溶液、“雪碧”饮料 |
 B.
B.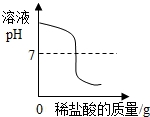 C.
C. D.
D.


 2Fe+3CO2
2Fe+3CO2