题目内容
12.同学们从山上采集到一种石灰石,他们取80g该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),反应结束后剩余固体的质量为75.6g.(1)当石灰石完全反应后,生成CO2的质量为4.4g.
(2)根据反应的化学方程式求该石灰石中CaCO3的质量为多少?写出计算过程.
分析 首先根据质量守恒定律得出固体质量减小的量即为生成的气体的质量,然后根据气体的质量可以求出样品中碳酸钙的质量.
解答 解:(1)由于固体的质量由80g变为75.6g,减少了4.4g,说明生成的气体的质量为4.4g;
(2)由于生成的气体的质量为4.4g,因此可以根据生成的气体的质量即可求出参与反应的碳酸钙的质量
设样品中含CaCO3的质量为x
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
x 4.4g
$\frac{100}{x}$=$\frac{44}{4.4g}$
x═10g
样品中的质量分数=$\frac{10g}{80g}$×100%=12.5%.
故答案为:(1)4.4g;
(2)样品中CaCO3的质量分数为12.5%.
点评 本题难度不是很大,主要考查了根据化学方程式进行相关的计算,从而培养学生的分析能力和计算能力.

练习册系列答案
相关题目
17.开封人不仅喜欢养菊花,赏菊花,而且还开发出菊花的加工品.菊花作为食品是因为里面有的营养物质是( )
| A. | 维生素 | B. | 蛋白质 | C. | 淀粉 | D. | 无机盐 |
1.有一种无色液体,不能使紫色石蕊试液变色,与AgNO3生成不溶于稀HNO3的白色沉淀,这无色溶液是( )
| A. | NaCl | B. | H2O | C. | HCl | D. | NaOH |
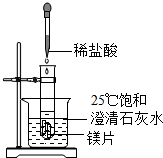 化学兴趣小组用如图装置进行实验,发现镁片完全溶解、石灰水浑浊.
化学兴趣小组用如图装置进行实验,发现镁片完全溶解、石灰水浑浊.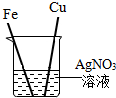 Fe,Cu.Ag是初中化学学过的三种金属,为探究它们的金属活动性顺序,将两支洁净的铁丝、铜丝分别插入足量的AgNO3溶液中.
Fe,Cu.Ag是初中化学学过的三种金属,为探究它们的金属活动性顺序,将两支洁净的铁丝、铜丝分别插入足量的AgNO3溶液中.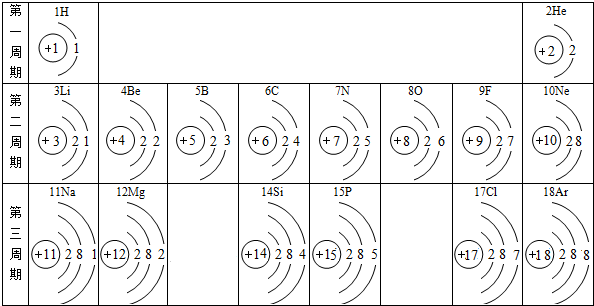
 化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成离子;
化学反应中该原子比较容易得到(填“得到”或“失去”)电子变成离子;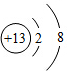 表示的是Al3+(填离子符号);
表示的是Al3+(填离子符号);