题目内容
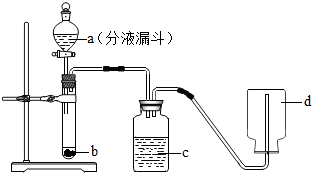
小亮同学在实验室中制取CO2气体后,对废液进行后续探究,他向一定质量的含CaCl2和HCl的溶液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液的质量与产生沉淀或者气体的质量关系如图1所示;加入Na2CO3溶液的质量与溶液的pH变化关系如图2所示.请回答:
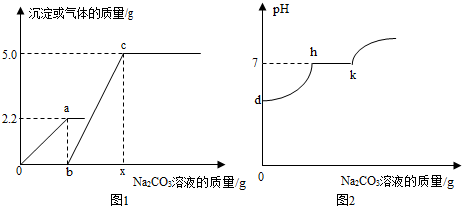
(1)图1中o→a段表示生成 (填“气体”或“沉淀”的过程).
(2)图1中ob线段与bx线段大小关系是 (填“<”、“>”或“=”).
(3)图1中a点时,溶液中的溶质化学式是 .
(4)图1中b~c段反应过程中溶液的pH变化情况可用图2中 (填“dh”或“hk”)段曲线表示.

(1)图1中o→a段表示生成
(2)图1中ob线段与bx线段大小关系是
(3)图1中a点时,溶液中的溶质化学式是
(4)图1中b~c段反应过程中溶液的pH变化情况可用图2中
考点:盐的化学性质,酸的化学性质,溶液的酸碱性与pH值的关系
专题:常见的酸 酸的通性,常见的盐 化学肥料
分析:根据加入的碳酸钠先与盐酸反应,把盐酸消耗完了,才开始与氯化钙反应,开始生成沉淀,最后到达最高点说明已经反应完了进行解答.
解答:解:(1)加入的碳酸钠先与盐酸反应,把盐酸消耗完了,才开始与氯化钙反应,开始生成沉淀,因此图中oa段表示生成的气体质量;
(2)根据题意可知碳酸钠先与盐酸反应,再与氯化钙反应,由图示可知碳酸钠与盐酸反应生成气体2.2g,碳酸钠与氯化钙反应,生成沉淀5.0g.设生成2.2g气体所需的Na2CO3的质量为y,生成沉淀5.0g所需Na2CO3的质量为z.则
Na2CO3+2HCl=2NaCl+CO2↑+H2O Na2CO3+CaCl2=CaCO3↓+2NaCl
106 44 106 100
y 2.2g z 5g
=
=
解得:y=5.3g z=5.3g
故ob线段与bx线段大小相等;
(3)a点表示碳酸钠先盐酸反应,把盐酸消耗完,故溶液中的溶质为氯化钠和氯化钙;
(4)当盐酸反应后,溶液中溶质有氯化钠和氯化钙,溶液呈中性,b~c段反应过程是碳酸钠与氯化钙反应,生成沉淀,在此过程中,溶液的PH不变,呈中性,故图1中b~c段反应过程中溶液的pH变化情况可用图2中hk段曲线表示.
故答案为:(1)气体;
(2)=;
(3)氯化钠和氯化钙;
(4)hk
(2)根据题意可知碳酸钠先与盐酸反应,再与氯化钙反应,由图示可知碳酸钠与盐酸反应生成气体2.2g,碳酸钠与氯化钙反应,生成沉淀5.0g.设生成2.2g气体所需的Na2CO3的质量为y,生成沉淀5.0g所需Na2CO3的质量为z.则
Na2CO3+2HCl=2NaCl+CO2↑+H2O Na2CO3+CaCl2=CaCO3↓+2NaCl
106 44 106 100
y 2.2g z 5g
| 106 |
| 44 |
| y |
| 2.2g |
| 106 |
| 100 |
| z |
| 5g |
解得:y=5.3g z=5.3g
故ob线段与bx线段大小相等;
(3)a点表示碳酸钠先盐酸反应,把盐酸消耗完,故溶液中的溶质为氯化钠和氯化钙;
(4)当盐酸反应后,溶液中溶质有氯化钠和氯化钙,溶液呈中性,b~c段反应过程是碳酸钠与氯化钙反应,生成沉淀,在此过程中,溶液的PH不变,呈中性,故图1中b~c段反应过程中溶液的pH变化情况可用图2中hk段曲线表示.
故答案为:(1)气体;
(2)=;
(3)氯化钠和氯化钙;
(4)hk
点评:解答本题关键要知道只有把盐酸反应完了,才能与氯化钙反应产生沉淀,因为如果碳酸钠与氯化钙先反应生成了碳酸钙沉淀,也会被剩余的盐酸溶解掉,将不会看到沉淀.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
桂林三宝指的是传统桂林土特产的代表,分别是:桂林三花酒、桂林辣椒酱、桂林豆腐乳.其中,属于溶液的是( )
| A、桂林三花酒 |
| B、桂林辣椒酱 |
| C、桂林豆腐乳 |
| D、以上都属于 |
下列有关氧气的说法正确的是( )
| A、氧气的约占空气体积的78% |
| B、硫在氧气中燃烧发出蓝紫色光 |
| C、工业分离液态空气制取氧气,是化学变化 |
| D、夏天温度升高,氧气在水中溶解度减少,鱼池内需开启增氧泵 |
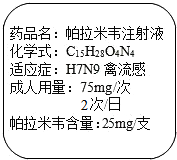 新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图.
新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图.