题目内容
2. 用如图所示装置测定空气中氧气的含量,其中集气瓶的容积为200mL,量筒的容量为250mL.实验步骤如下(装置气密性良好):
用如图所示装置测定空气中氧气的含量,其中集气瓶的容积为200mL,量筒的容量为250mL.实验步骤如下(装置气密性良好):I.打开止水夹a和b,向集气瓶中缓慢鼓入一定量空气,稍后,测得进入到量筒中的水的体积为V1mL;
II.用强光手电照射,引燃红磷;
III.红磷熄灭并冷却至室温,打开止水夹b,测得量筒中的水的体积变为V2mL;
IV.计算空气中氧气的体积分数.
(1)红磷燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)整个实验过程中的现象为鼓入空气时集气瓶中大部分水排入量筒中,红磷燃烧产生大量白烟,冷却后打开b,量筒中的水进入集气瓶中.
(3)步骤Ⅱ中引燃红磷前应进行的操作是关闭止水夹a和b,否则会影响测定结果.
(4)步骤III中,未冷却至室温会使测得的V2数值偏高(填“没有影响”、“偏高”或“偏低”).
分析 红磷在空气中燃烧生成五氧化二磷,产生大量白烟,放出热量;
集气瓶中的氧气消耗后,压强减小,量筒中的水会进入集气瓶中.
解答 解:(1)红磷燃烧的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
故填:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)整个实验过程中的现象为:鼓入空气时集气瓶中大部分水排入量筒中,红磷燃烧产生大量白烟,冷却后打开b,量筒中的水进入集气瓶中.
故填:鼓入空气时集气瓶中大部分水排入量筒中,红磷燃烧产生大量白烟,冷却后打开b,量筒中的水进入集气瓶中.
(3)步骤Ⅱ中引燃红磷前应进行的操作是关闭止水夹a和b,否则集气瓶中的气体会受热逸出,会影响测定结果.
故填:关闭止水夹a和b.
(4)步骤III中,未冷却至室温就打开止水夹b,会导致进入集气瓶中的水偏少,从而导致测得的V2数值偏高.
故填:偏高.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
12.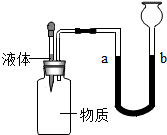 下列各组物质能按右图所示装置进行实验.当胶头滴管中的液体滴入瓶中,U型管中的液面发生了明显变化.若a处液面上升,b处液面降低,则符合此现象的物质组合的是( )
下列各组物质能按右图所示装置进行实验.当胶头滴管中的液体滴入瓶中,U型管中的液面发生了明显变化.若a处液面上升,b处液面降低,则符合此现象的物质组合的是( )
 下列各组物质能按右图所示装置进行实验.当胶头滴管中的液体滴入瓶中,U型管中的液面发生了明显变化.若a处液面上升,b处液面降低,则符合此现象的物质组合的是( )
下列各组物质能按右图所示装置进行实验.当胶头滴管中的液体滴入瓶中,U型管中的液面发生了明显变化.若a处液面上升,b处液面降低,则符合此现象的物质组合的是( )| 液体 | 物质 | |
| A | 澄清石灰水 | CO2气体 |
| B | H2O | 氧化钙 |
| C | 稀硫酸 | 铁片 |
| D | 双氧水 | 二氧化锰 |
| A. | A | B. | B | C. | C | D. | D |
13.将80g溶质质量分数为20%的盐酸加水稀释成10%的盐酸,需加入水的质量为( )
| A. | 280g | B. | 100g | C. | 80g | D. | 200 g |
10.下列说法正确的是( )
| A. | 由不同种元素组成的物质一定是混合物 | |
| B. | 某物质能与碱反应生成盐和水,则该物质一定是酸 | |
| C. | 向某固体中加入稀盐酸有气体产生,则该固体一定是较活泼金属 | |
| D. | 饱和溶液析出晶体后,溶质质量分数不一定减小 |
14.大蒜中含有的一种有效成分“硫化丙烯”(C3H6S)具有一定的杀菌食疗作用.下列有关硫化丙烯的说法正确的是( )
| A. | 硫化丙烯分子由3个碳元素、6个氢元素和1个硫元素构成 | |
| B. | 硫化丙烯中硫元素的质量分数最大 | |
| C. | 硫化丙烯分子中碳、氢、硫元素质量比为3:6:1 | |
| D. | 74g硫化丙烯中硫元素的质量为32g |
9.鉴别空气、氧气和二氧化碳三瓶气体的正确方法是( )
| A. | 闻气体的气味 | B. | 分别插入燃着的木条 | ||
| C. | 观察气体的颜色 | D. | 分别倒入少量的澄清石灰水 |
10.下列化学用语中,正确的是( )
| A. | 2个氧分子:2O | B. | 氧化钠:NaO | C. | 一氧化碳:Co | D. | 3个钠离子:3Na+ |
 水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.
水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任. 有A、B、C、D四种物质,其中B是建筑材料的主要成分:C是引起温室效应的主要气体;D与A、B均发生复分解反应.它们之间的相互关系如图所示(“→”表示物质间的转化关系,“-”表示物质间可以相互反应),请回答下列问题:
有A、B、C、D四种物质,其中B是建筑材料的主要成分:C是引起温室效应的主要气体;D与A、B均发生复分解反应.它们之间的相互关系如图所示(“→”表示物质间的转化关系,“-”表示物质间可以相互反应),请回答下列问题: