题目内容
4.按要求写出下列变化的化学方程式.(1)三氧化硫与氢氧化钠溶液充分反应:2NaOH+SO3=Na2SO4+H2O;
(2)纯碱溶液与饱和石灰水反应:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(3)服用含氢氧化铝[Al(OH)3]的药物可以治疗胃酸过多症:Al(OH)3+3HCl=AlCl3+3H2O.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写.
解答 解:(1)由题意,可知三氧化硫与氢氧化钠溶液反应的反应物和生成物,故化学方程式为SO3+2NaOH═Na2SO4+H2O;
(2)纯碱溶液与石灰水反应生成碳酸钙和氢氧化钠,注意沉淀符号的书写.该反应的化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)氢氧化铝与胃液中的盐酸反应生成氯化铝和水,反应的化学方程式是Al(OH)3+3HCl═AlCl3+3H2O;
故答案为:
(1)2NaOH+SO3=Na2SO4+H2O
(2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
(3)Al(OH)3+3HCl=AlCl3+3H2O
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
14.用化学用语填空.
(1)2 个氢分子2H2
(2)5个镁离子5Mg2+
(3)氧化铜中铜元素的化合价$\stackrel{+2}{Cu}$O.
(4)地壳中含量最多的金属元素Al
(5)纯碱Na2CO3.
(1)2 个氢分子2H2
(2)5个镁离子5Mg2+
(3)氧化铜中铜元素的化合价$\stackrel{+2}{Cu}$O.
(4)地壳中含量最多的金属元素Al
(5)纯碱Na2CO3.
15.如图1所示中的实验方法或操作正确的是( )
| A. | 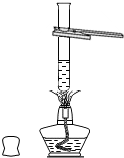 加热液体 | B. | 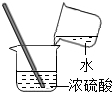 稀释浓硫酸 | ||
| C. | 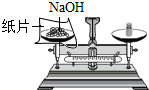 称量氢氧化钠固体 | D. | 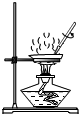 蒸发食盐水 |
19.下表是某同学用多种方法对物质进行提纯或鉴别的情况,其中两种方法均正确的是( )
| 选项 | 实验目的 | 方法和所加试剂 | |
| 方法一 | 方法二 | ||
| A | 除去氯化钠溶液中少量氢氧化钠 | 滴加稀盐酸至pH等于7 | 滴加适量硫酸铜 |
| B | 除去CO2中少量的HCl气体 | 通过NaOH溶液、浓硫酸 | 通过NaOH固体 |
| C | 鉴别硝酸铵固体和氢氧化钠固体 | 加入熟石灰、研磨 | 滴加水 |
| D | 鉴别稀烧碱溶液和石灰水 | 滴加酚酞溶液 | 加入氯化铁溶液 |
| A. | A | B. | B | C. | C | D. | D |
16.工厂为防止环境污染和回收贵重金属,向含有Cu(NO3)2和AgNO3的废液中加入一定量的铁粉,充分反应后过滤,得到滤液和滤渣,滤渣中加入稀盐酸,发现有气泡产生,根据上述现象的描述,下列四种判断正确的是( )
| A. | 滤渣中一定有Ag、Cu、Fe | |
| B. | 滤渣中一定有Ag和Cu,可能含有Fe AgNO3和Cu(NO3)2 | |
| C. | 滤液中一定有含Fe(NO3)2,可能含有AgNO3和Cu(NO3)2 | |
| D. | 滤液中一定含有AgNO3和Cu(NO3)2,可能含有含Fe(NO3)2 |
17.漂白粉在生活中有重要的应用,氯气与石灰乳反应制成漂白粉的化学方程式为2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2X,其中X的化学式是( )
| A. | CaO | B. | H2O2 | C. | H2O | D. | HClO |
 小坤同学发现他家养的鲜花植株矮小,茎秆很细,叶片,发黄,便利用所学知识施加了如图包装袋所示的化肥.计算回答下列问题:
小坤同学发现他家养的鲜花植株矮小,茎秆很细,叶片,发黄,便利用所学知识施加了如图包装袋所示的化肥.计算回答下列问题: