题目内容
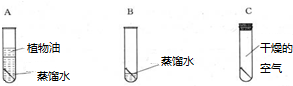
9. 电解水实验:a管中产生30mL的气体时,b管中同时产生气体15mL,如何检验b管中产生的气体将带火星的木条放入试管中,观察是否复燃;电解水的实验说明水是由氢元素和氧元素组成,反应的符号表达式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该反应属于分解反应.
电解水实验:a管中产生30mL的气体时,b管中同时产生气体15mL,如何检验b管中产生的气体将带火星的木条放入试管中,观察是否复燃;电解水的实验说明水是由氢元素和氧元素组成,反应的符号表达式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该反应属于分解反应.
分析 由正氧负氢,氢二氧一可知电解水时正极产生氧气,可用带火星的木条检验,负极产生氢气能燃烧,氢气和氧气的体积比为2:1,化学反应前后元素的种类不变可判断物质的元素组成.
解答 解:电解水时氢氧两种气体的体积比是2:1,由实验的装置可知,a管中产生的气体是电源的负极产生的气体是氢气,若产生30mL的氢气时,b管中同时产生气体15mL的氧气,氧气能使带火星的木条复燃,检验方法是:将带火星的木条放入试管中,观察是否复燃;利用生成物的元素组成结合质量守恒定律可知水是由氢氧两种元素组成的,反应化学方程式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该反应由一种物质生成了两种物质,属于分解反应.
故答案为:15 将带火星的木条放入试管中,观察是否复燃 氢元素和氧元素; 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,分解.
点评 】此题是对水的电解的考查,解题的关键是掌握水电解时的现象及证明的问题,属基础性知识考查题.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目