题目内容
3.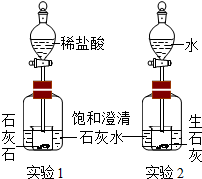 如图,实验一和实验二都会观察到的现象是澄清的石灰水变浑浊.实验一产生这一现象的原因是石灰石和稀盐酸反应生成了二氧化碳,二氧化碳与石灰水中的氢氧化钙反应生成了不溶于水的碳酸钙.实验二产生这一现象的原因是生石灰和水反应放出大量的热使石灰水的温度上升,石灰水中的氢氧化钙的溶解度随着温度的升高而减小,有Ca(OH)2固体析出.
如图,实验一和实验二都会观察到的现象是澄清的石灰水变浑浊.实验一产生这一现象的原因是石灰石和稀盐酸反应生成了二氧化碳,二氧化碳与石灰水中的氢氧化钙反应生成了不溶于水的碳酸钙.实验二产生这一现象的原因是生石灰和水反应放出大量的热使石灰水的温度上升,石灰水中的氢氧化钙的溶解度随着温度的升高而减小,有Ca(OH)2固体析出.
分析 稀盐酸与石灰石反应生成二氧化碳,二氧化碳能使澄清的石灰水边浑浊.生石灰遇水发生放热反应,则石灰水的温度升高,所以从氢氧化钙的溶解度受温度影响的方面进行考虑.
解答 解:实验1中,石灰石和稀盐酸反应生成了二氧化碳,二氧化碳与石灰水中的氢氧化钙反应生成了不溶于水的碳酸钙;
实验2中,生石灰和水反应放出大量的热使石灰水的温度上升,石灰水中的氢氧化钙的溶解度随着温度的升高而减小,有Ca(OH)2固体析出.
故答案是:澄清的石灰水变浑浊;石灰石和稀盐酸反应生成了二氧化碳,二氧化碳与石灰水中的氢氧化钙反应生成了不溶于水的碳酸钙;生石灰和水反应放出大量的热使石灰水的温度上升,石灰水中的氢氧化钙的溶解度随着温度的升高而减小,有Ca(OH)2固体析出.
点评 澄清石灰水通入二氧化碳变浑浊,实验室通常利用这一变化检验气体是不是二氧化碳.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列有关物质的检验方法和结论都合理的是( )
| A. | 加入稀盐酸,有无色气体产生的物质中一定含有碳酸盐 | |
| B. | 用燃着的木条伸入某气体中,火焰熄灭,则该气体一定是二氧化碳 | |
| C. | 经点燃,产生蓝色火焰的气体一定是一氧化碳 | |
| D. | 某溶液中加入稀盐酸无任何明显现象,再加入氧化钡溶液,出现白色沉淀,则原来溶液中一定含有硫酸根离子 |
12.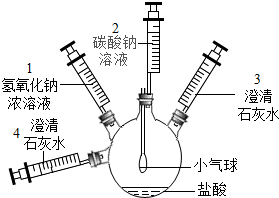 某实验小组设计了如图实验装置及方案,实验步骤如下,请回答有关问题:
某实验小组设计了如图实验装置及方案,实验步骤如下,请回答有关问题:
第一步:注射器2中的溶液推入盛有稀盐酸烧瓶中,至不再有气泡产生,实验现象是小气球慢慢变瘪.
第二步:注射器 3 稍稍向外拉澄清石灰水变浑浊,反应方程式是CO2+Ca(OH)2═CaCO3↓+H2O.
第三步:注射器 1 中的溶液推入瓶中,气体鼓起
第四步:要证明瓶内气体被吸收完全的操作方法和判断依据是将注射器4稍稍向外拉,若澄清石灰水无明显现象,则证明瓶内气体被吸收完全.
第五步:注射器 4 中的溶液推入瓶中,反应方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
第六步:完成上述实验后,小刘继续对瓶内溶液的成分进行了探究:
①提出猜想:溶液的溶质中一定含有 NaOH 和 NaCl,可能含有氢氧化钙或碳酸钠.
②实验验证:设计实验方案确定溶液中是否含有氢氧化钙,请补充完整下列
实验报告:二氧化碳能与氢氧化钠反应生成碳酸钠.
 某实验小组设计了如图实验装置及方案,实验步骤如下,请回答有关问题:
某实验小组设计了如图实验装置及方案,实验步骤如下,请回答有关问题:第一步:注射器2中的溶液推入盛有稀盐酸烧瓶中,至不再有气泡产生,实验现象是小气球慢慢变瘪.
第二步:注射器 3 稍稍向外拉澄清石灰水变浑浊,反应方程式是CO2+Ca(OH)2═CaCO3↓+H2O.
第三步:注射器 1 中的溶液推入瓶中,气体鼓起
第四步:要证明瓶内气体被吸收完全的操作方法和判断依据是将注射器4稍稍向外拉,若澄清石灰水无明显现象,则证明瓶内气体被吸收完全.
第五步:注射器 4 中的溶液推入瓶中,反应方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
第六步:完成上述实验后,小刘继续对瓶内溶液的成分进行了探究:
①提出猜想:溶液的溶质中一定含有 NaOH 和 NaCl,可能含有氢氧化钙或碳酸钠.
②实验验证:设计实验方案确定溶液中是否含有氢氧化钙,请补充完整下列
| 实验操作 | 实验现象 | 实验结论 |
| 取少量瓶内溶液于试管中,加入碳酸钠溶液,振荡 | 有白色沉淀生成 | 瓶内溶液中溶质的成分含有氢氧化钙 |
 实验室有一瓶标签被腐蚀的盐酸,为测定溶液中溶质的质量分数,在烧杯中配制了8g10%的NaOH溶液,然后往烧杯中滴加该盐酸,反应过程中溶液的pH与滴入盐酸的质量关系如图所示.请回答下列问题:
实验室有一瓶标签被腐蚀的盐酸,为测定溶液中溶质的质量分数,在烧杯中配制了8g10%的NaOH溶液,然后往烧杯中滴加该盐酸,反应过程中溶液的pH与滴入盐酸的质量关系如图所示.请回答下列问题: A-F表示初中化学常见的物质,且A、B、C属于不同类别的物质.A和B,B和C都能发生反应,都只能生成两种产物,它们之间转化关系如图所示.
A-F表示初中化学常见的物质,且A、B、C属于不同类别的物质.A和B,B和C都能发生反应,都只能生成两种产物,它们之间转化关系如图所示.