题目内容
11.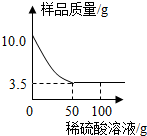 某化学兴趣小组对某铜锌合金样品进行探究实验.称取样品10.0克,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示.求:
某化学兴趣小组对某铜锌合金样品进行探究实验.称取样品10.0克,再用100.0克稀硫酸溶液逐滴滴入,实验情况如图所示.求:(1)铜锌合金中,Zn的质量分数是65%.
(2)所用稀硫酸溶液中溶质的质量分数是多少?
分析 根据题意,锌与稀硫酸反应生成硫酸锌和氢气;由反应的实验情况图,完全反应后剩余固体的质量为3.5g,即铜锌合金样品中含铜的质量为3.5g;则锌的质量为10g-3.5g=6.5g;由参加反应的锌的质量,计算出参加反应硫酸的质量,进而可计算出所用稀硫酸溶液中溶质的质量分数.
解答 解:(1)由反应的实验情况图,完全反应后剩余固体的质量为3.5g,即铜锌合金样品中含铜的质量为3.5g,则锌的质量为10g-3.5g=6.5g.
铜锌合金中,Zn的质量分数是$\frac{6.5g}{10.0g}×$100%=65%.
(2)设反应中消耗稀硫酸溶液中溶质的质量为x,
Zn+H2SO4═ZnSO4+H2↑
65 98
6.5g x
$\frac{65}{98}$=$\frac{6.5g}{x}$ x=9.8g
所用稀硫酸溶液中溶质的质量分数为:$\frac{9.8g}{50g}×$100%=19.6%.
答:所用稀硫酸溶液中溶质的质量分数是19.6%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析图表信息,确定铜的质量为3.5g的质量是正确解答本题的前提和关键.

练习册系列答案
相关题目
1.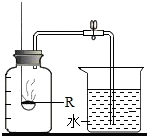 用如图装置测定空气中氧气的含量,物质R应该选用( )
用如图装置测定空气中氧气的含量,物质R应该选用( )
 用如图装置测定空气中氧气的含量,物质R应该选用( )
用如图装置测定空气中氧气的含量,物质R应该选用( )| A. | 红磷 | B. | 硫粉 | C. | 木炭 | D. | 铁片 |
16.如图是某个化学反应的微观示意图.下列从图中获得的有关信息正确的是( )
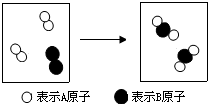

| A. | 反应物含3种元素 | B. | 生成了2种物质 | ||
| C. | 反应前后元素种类不变 | D. | 反应前后分子个数不变 |
3.明确宏观现象的微观本质是学习化学的重要思想方法,下列说法正确的是( )
| A. | 水与冰的共存物是纯净物,是因为它们由同种分子构成 | |
| B. | 水结成冰,是因为温度降低,分子停止运动 | |
| C. | 水通电分解生成氢气和氧气,是因为水中含有氢分子和氧分子 | |
| D. | 水与酒精混合液的体积小于混合前二者体积之和,是因为混合后分子体积变小 |
 .
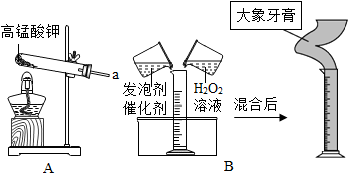
.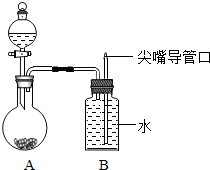 如图是某同学设计的趣味小实验装置,其气密性良好,若要使B中尖嘴导管处有“喷泉”产生,则A中加入的固体和液体物质可能是( )
如图是某同学设计的趣味小实验装置,其气密性良好,若要使B中尖嘴导管处有“喷泉”产生,则A中加入的固体和液体物质可能是( )